Перегруппировка - перэфир
Cтраница 1
Перегруппировка перэфиров ускоряется добавками кислот. Из этой таблицы видно, что значительное повышение кислотности среды сравнительно мало увеличивает скорость перегруппировки кумилпербензоата. Имеет место линейная зависимость константы скорости этой реакции от концентрации добавленной серной кислоты. [1]
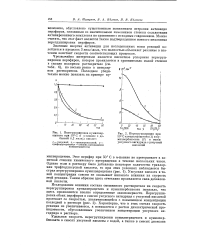
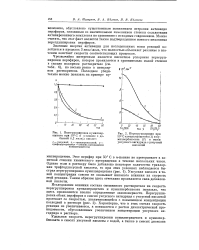
Чрезвычайно интересным является кислотное ускорение перегруппировки перэфиров, которое проявляется в сравнительно малой степени в сильно полярном растворителе ( см. табл. 6), но весьма резко в неполяр-ном растворителе. [3]
Можно считать, что этот факт является также подтверждением ионного механизма перегруппировки перэфиров. [5]
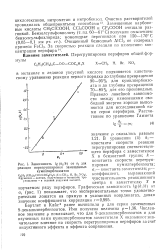 |
Зависимость lg ( ki / k от а. для. [6] |
Численное значение р показывает, что для 9-декалилпербензоатов и для изученных нами кумилпербензоатов заместители X оказывают значительное влияние на скорость перегруппировки перэфиров за счет индуктивного эффекта и эффекта сопряжения. [7]
Это означает, что образование водородного мостика между молекулой растворителя и карбонильным кислородом перэфира оказывает значительно более сильное действие на поляризацию связи О-О и соответственно на скорость перегруппировки перэфира, чем диполь-дипольное взаимодействие в случае неспецифического эффекта сольватации. Как видно из данных табл. 2, численные значения кажущейся энергии активации Е реакции перегруппировки кумилпербензоата лежат в пределах 20 7 - 22 6 ккал / моль, в то время как константы скорости реакции различаются весьма значительно. Скорость перегруппировки с изменением природы растворителя определяется в основном изменением энтропии активации. [8]
Перегруппировка - перэфиров в очень сильной степени зависит как от природы перекисной группы, так и от природы кислотного остатка. Литературные данные, а также наши результаты, показывают, что чем более сильной кислоты кислотный остаток входит в состав перэфира, тем больше скорость его перегруппировки. С другой стороны, чем больше фснильных групп у атома углерода, связанного с перекисным кислородом, тем легче также идет перегруппировка перэфира. Этим объясняются неудачные попытки синтезировать трифенилметилпербензоат и кумил - / г-нитропер-бензоат. [9]
Кумилперацетат в чистом состоянии при 90 С довольно быстро перегруппировывается без выделения двуокиси углерода. В растворе Кумилперацетат разлагается со скоростью, сильно различающейся в зависимости от природы растворителя. Так, например, в w - нонане это соединение даже при 90 С разлагается настолько медленно, что в течение трех часов при этих условиях в растворе мы не обнаружили никакого понижения концентрации перекисного кислорода. При тех же условиях Кумилперацетат разлагается со значительной скоростью в нитробензоле и в уксусном ангидриде и с очень большой скоростью - в уксусной кислоте, а также в ее смеси с водой. Эта реакция представляет собою гетеролити-ческую перегруппировку перэфира в соединение, легко гидролизующееся водой с образованием ацетона, фенола и уксусной кислоты. Выход ацетона и уксусной кислоты количественный, фенола - 93 - 95 % от теоретически рассчитанного количества. [10]
Таким образом, о механизме данной перегруппировки нет еще достаточно надежно подтвержденного единого мнения. В настоящем сообщении изложены результаты исследования кинетики гетеролитической перегруппировки кумилпербензоата и некоторых его производных. Особое внимание при этом обращено на зависимость скорости реакции от природы заместителя в перэфире и от ионизирующей силы среды, а также от природы катализатора. Одновременно с этим было проведено масс-спектрометрическое исследование с целью установления существования ионных пар в реакциях перегруппировки перэфиров. [11]
Таким образом, о механизме данной перегруппировки нет еще достаточно надежно подтвержденного единого мнения. В настоящем сообщении изложены результаты исследования кинетики гетеролитической перегруппировки кумилпербензоата и некоторых его производных. Особое внимание при этом обращено на зависимость скорости реакции от природы заместителя в перэфире и от ионизирующей силы среды, а также от природы катализатора. Одновременно с этим было проведено масс-спектрометрическое исследование с целью установления существования ионных пар в реакциях перегруппировки перэфиров. [12]
Страницы: 1