Большинство - промышленный катализатор
Cтраница 1
Большинство промышленных катализаторов являются пористыми телами: куски катализатора пронизаны по всем направлениям громадным количеством пор - каналов различной формы и размеров. Поверхность этих пор часто в десятки тысяч раз превышает величину внешней, геометрической поверхности куска. Вся эта поверхность каталитически активна, но доступность ее для реагирующих веществ неодинакова: чем глубже внутри куска лежит данный участок поверхности, тем труднее осуществляется диффузия к ней веществ сквозь поры. [1]
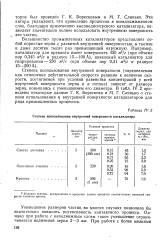 |
Степень использования внутренней поверхности катализатора. [2] |
Большинство промышленных катализаторов представляет собой пористые зерна с развитой внутренней поверхностью, в тысячи и даже десятки тысяч раз превышающей наружную. [3]
Большинство промышленных катализаторов состоит из пористых зерен с развитой внутренней поверхностью, обычно в десятки тысяч раз превышающей внешнюю поверхность, непосредственно омываемую газовым потоком. Скорость переноса реагирующих веществ к этой внутренней поверхности оказывает поэтому особенно большое влияние на протекание контактных процессов. [4]
Большинство промышленных катализаторов, и в том числе ванадиевые сернокислотные, представляют собой пористые вг-щества с высокоразвитым внутренним объемом. Их каталитическая активность зависит от удельной активности поверхности и степени доступности этой поверхности. [5]
Большинство промышленных катализаторов представляет собой пористые зерна с развитой внутренней поверхностью, в тысячи и даже десятки тысяч раз превышающей наружную. [6]
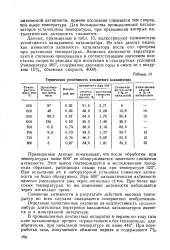 |
Термическая устойчивость ванадиевого катализатора. [7] |
Для большинства промышленных катализаторов установлены температуры, при превышении которых каталитическая активность снижается. [8]
Высокая каталитическая активность большинства промышленных катализаторов обусловлена большой величиной внутренней поверхности, достигающей сотен квадратных метров на грамм катализатора. Подобрав оптимальную внутреннюю структуру, можно изготовить активные катализаторы из материалов, обладающих умеренной активностью, отнесенной к единице поверхности. Однако одно увеличение внутренней поверхности катализатора не всегда приводит к росту его активности, а иногда может сопровождаться даже снижением выхода полезного продукта. Каждому контактному процессу отвечает определенная оптимальная внутренняя структура, зависящая от условий проведения процесса и скорости реакции. [9]
Обычная скорость образования углерода на большинстве промышленных катализаторов составляет в этих условиях около 1 2 г углерода в час на кг катализатора. Катализатор 41 - 4 является модификацией, специально разработанной для уменьшения образования углерода и соответствующей дезактивации в процессе работы. При использовании этого катализатора уменьшается необходимость в регенерации посредством обработки паром или водородом. Однако некоторое отложение углерода имеет место на всех катализаторах этого типа, что особенно заметно при одновременном применении низкого давления и высокой температуры. Удельная скорость образования углерода на катализаторе 41 - 4 составляет 0 33 г / кг. [10]
Активность катализаторов, описанных и докладе () 2, а также большинства промышленных катализаторов почти не зависит от размеров частиц ( площади) твердой фазы в широком интервале их изменения. Она не зависит также от присутствия известных инертных носителей. Следовательно, активность катализаторов определяется собственными свойствами их поверхности. Однако совмещение двух или нескольких твердых фаз может приводить к образованию на границе раздела новой фаяы. Поэтому при создании катализатора необходимо учитывать соответствующие химические свойства компонентов. Некоторые легкоплавкие, летучие окислы, например МоО), легко образуют подобные соединения с другими компонентами. В настоящее время рассмотрение свойств границ раздела не представляется актуальным. [11]
Эта величина используется в уравнениях, предназначенных для оценки скорости реакций в порах, так как большинство промышленных катализаторов прессуется в виде таблеток, имеющих сферическую или цилиндрическую форму, вся внешняя поверхность которых подвергается действию реагирующего газа. [12]
Тех условий, которые существовали при потенциометрических исследованиях, проводившихся с целью показать образование центров основного обмена, не имеется при получении большинства промышленных катализаторов крекинга, хотя описанные выше явления, несомненно, и здесь играют важную роль. Как уже указывалось, в производстве многих шариковых и микросферических катализаторов гидролиз соли алюминия обычно проводят в присутствии геля SiOa, уже полимеризованного при старении. Если гель окиси кремния подвергался старению значительное время, кривая титрования поднимается вверх и достигает точки, которая соответствует соосаждению гидроокиси алюминия. В этом случае, для нейтрализации требуется только три эквивалента щелочи на 1 моль алюминия. [13]
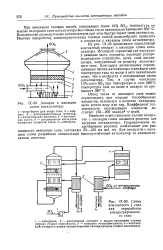 |
Аппарат с кипящим слоем катализатора.| Х-50. Схема контактного узла CQ для переработки. [14] |
При окислении газовых смесей, содержащих более 10 % SO2, температура на выходе из первого слоя катализатора без отвода тепла значительно превышает 600 С. Большинство промышленных катализаторов при этом быстро теряет свою активность. [15]
Страницы: 1 2 3