Большинство - кислота
Cтраница 2
 |
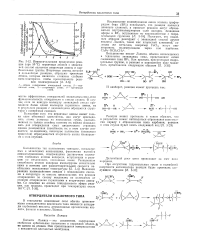
Результаты определения первичных, алифатических аминов в присутствии других аминов по реакции с ацетилацетоном. [16] |
Большинство кислот, а также основания с константой ионизации выше ЫО 2, мешают определению аминов описанным методом. Так как метод основан на неводном титровании, наличие в значительном количестве воды обусловливает известную неопределенность эквивалентной точки. Обычно допускается до 10 % воды. [17]
Большинство кислот достаточно хорошо растворимо в воде и практически нерастворимо в спирте и ди-этиловом эфире, что указывает на солеобразный характер этих веществ. [18]
 |
Результаты определения первичных, алифатических аминов в присутствии других аминов по реакции с ацетилацетоном. [19] |
Большинство кислот, а также основания с константой ионизации выше ЫО 2, мешают определению аминов описанным методом. Так как метод основан на неводном титровании, наличие в значительном количестве воды обусловливает известную неопределенность эквивалентной точки. Обычно допускается до 10 % воды. [20]
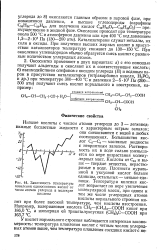 |
Зависимость температуры. [21] |
Большинство кислот Q - С8 - масляные жидкости с неприятным запахом. Растворимость их в воде сильно уменьшается по мере возрастания молекулярных масс. Кислоты от С ] 0 и выше - твердые вещества, нерастворимые в воде. [22]
Большинство кислот Льюиса представляют собой многоэлектронные молекулы или катионы, однако протон, который также относится к кислотам Льюиса, не имеет ин одного электроив. Кроме того, протон очень мал по размерам и, следовательно, способен очень быстро двигаться, т.е. кислотно-основные реакции в участием протоив часто могут идти очень быстро. Таким образом, протон среди кислот должен занимать особое место. Выделение протона из всех кислот Льюиса обусловлено также и его особой ролью в органической химии и биохимии. Протон является также исключительно эффективным катализатором многих реакций, происходящих в гидроксилсодержащих растворителях ( воде, спиртах, карбоновых кислотах и т.п.), например, гидролиза простых и сложных эфиров, этерификации карбоновых кислот, гидратации олефинов, альдольной конденсации и многих других. Особая роль протона как кислоты подчеркивается в теории кислот и оснований Бренстеда. [23]
Большинство кислот Льюиса, обычно используемых в технологии эпоксидных смол, представляют собой соединения типа ВРз. [25]
Поскольку большинство кислот при выполнении этого метода количественно титруются основанием, то, следовательно, может быть введена соответствующая поправка. [26]
Действие большинства кислот почти не отличимо от действия среды, в которой нет дикарбоновой кислоты. [27]
К действию большинства кислот углеродистые стали не устойчивы. В концентрированных окислительных кислотах, например серной и азотной, стойкость сталей повышается вследствие пассивности. К действию щелочей при обычной температуре углеродистая сталь стойка; при высоких температурах наблюдается растрескивание. [28]
 |
Результаты титрования гексаметилентетрамина хлорной кислотой. [29] |
Степень ионизации большинства кислот и оснований в диоксане и других растворителях с низкой диэлектрической проницаемостью очень невелика ( исключение составляют растворители с заметными кислотными или основными свойствами), поэтому следует ожидать, что в таких средах ацидиметрическое титрование с участием ионов будет протекать медленно с нерезко выраженной конечной точкой титрования. Однако все основания, которые хорошо титруются в диоксане, нейтральны и не реагируют в ионном состоянии. [30]
Страницы: 1 2 3 4