Большинство - тяжелый металл
Cтраница 1
Большинство тяжелых металлов мало реагирует на холоду с разбавленной С. SOa и одновременно дают сульфаты. На золото, платину, иридий и родий С. Чугун мало разъедается С. Лунге [8] тщательно исследовал коррозийное действие С. [1]
Большинство тяжелых металлов образует с дитиолом труднорастворимые соединения [39], которые не экстрагируются в условиях экстракции дитиолата молибдена. [2]
Хроматы большинства тяжелых металлов малорастворимы в воде. [3]
Поскольку перхлораты большинства тяжелых металлов относительно растворимы, хлорная кислота и ее соли часто применяются в таких процессах окончательной отделки металлов, как гальваностегия, травление и полирование. Например, согласно Яквету и Роквету29, сталь почти всех марок может быть отполирована, причем с поверхности металла удаляется вся пленка окиси. Для этого очищаемый металл помещают в качестве анода в ванну с уксусным ангидридом и хлорной кислотой, поддерживаемую при температуре ниже 30 С; катодом может служить стальная или алюминиевая пластины. Металл, вынутый из ванны, покрыт слоем красновато-коричневого вязкого осадка, легко удаляемого промывкой. Для полировки алюминия Окада30 рекомендует применять 20 % - ную хлорную кислоту в 50 % - ном спирте или только 75 % - ную хлорную кислоту при высокой плотности тока. [4]
Осаждение гидроокисей большинства тяжелых металлов в процессе проведения анализа предотвращают, связывая их в комплекс этилендиа-минтетрауксусной кислотой. Комплексное соединение серебра с этиленди-аминтетрауксусной кислотой настолько слабо, что практически не увеличивает растворимости роданата серебра. [5]
Поскольку перхлораты большинства тяжелых металлов относительно растворимы, хлорная кислота и ее соли часто применяются в таких процессах окончательной отделки металлов, как гальваностегия, травление и полирование. Например, согласно Яквету и Роквету29, сталь почти всех марок может быть отполирована, причем с поверхности металла удаляется вся пленка окиси. Для этого очищаемый металл помещают в качестве анода в ванну с уксусным ангидридом и хлорной кислотой, поддерживаемую при температуре ниже 30 С; катодом может служить стальная или алюминиевая пластины. Металл, вынутый из ванны, покрыт слоем красновато-коричневого вязкого осадка, легко удаляемого промывкой. Для полировки алюминия Окада30 рекомендует применять 20 % - ную хлорную кислоту в 50 % - ном спирте или только 75 % - ную хлорную кислоту при высокой плотности тока. [6]
Часто используют отделение большинства тяжелых металлов с помощью пиролидиндитиокарбамината натрия [228]; титан при этом остается в водном растворе. [7]
Кобальтицианид калия образует с большинством тяжелых металлов характерно окрашенные, трудно растворимые или совсем нерастворимые соли. [8]
Мы уже знаем, что аммиакаты большинства тяжелых металлов относительно устойчивы в водном растворе, а аммиакаты щелочных и щелочноземельных металлов разлагаются при растворении в воде. Это объясняется тем, что при взаимодействии относящихся к типу инертного газа ионов щелочных и щелочноземельных металлов с водой главную роль играет перманентный диполь молекулы воды. Между тем перманентный диполь-ный момент воды ( 1 7 - 1018) больше, чем аммиака ( 1 44 - 1018), а явления поляризации играют здесь относительно небольшую роль. Наоборот, при взаимодействии ионов неблагородногазового типа с дипольными молекулами главную роль играют индуцированные диполи, и так как поляризуемость аммиака, измеряемая его молекулярной рефракцией, значительно больше, чем у воды, то наблюдаемые на опыте соотношения оказываются совершенно естественными. Ван-Аркель и де - Бур 6 вычислили, что при образовании иона [ AgNH3 ] выделяется 49 ккал, а при образовании иона [ AgH2O ] 41 5 ккал. Если не принимать во внимание поляризации, то гидрат должен был бы быть прочнее. Если учитывать только заряд и перманентный диполь NH3 и не принимать во внимание поляризуемости Ag, то при образовании иона [ AgNHg ] 1 должно выделиться всего 40 ккал. Разумеется, если ион типа инертного газа обладает благоприятным соотношением заряда и радиуса, то его поляризующее действие может достигнуть столь больших размеров, что он все-таки будет давать аммиакаты в водном растворе. [9]
Мы уже знаем, что аммиакаты большинства тяжелых металлов относительно устойчивы в водном растворе, а аммиакаты щелочных и щелочноземельных металлов разлагаются при растворении в воде. Это объясняется тем, что при взаимодействии относящихся к типу инертного газа ионов щелочных и щелочноземельных металлов с водой главную роль играет перманентный диполь молекулы воды. Между тем перманентный дпполь-ный момент воды ( 1 7 - 1018) больше, чем аммиака ( 1 44 - 1018), а явления поляризации играют здесь относительно небольшую роль. Наоборот, при взаимодействии ионов неблагородногазового типа с дипольными молекулами главную роль играют индуцированные диполи, п так как поляризуемость аммиака, измеряемая его молекулярной рефракцией, значительно больше, чем у воды, то наблюдаемые на опыте соотношения оказываются совершенно естественными. Ван-Аркель и де - Бур 6 вычислили, что при образовании иона [ AgNH3 ] выделяется 49 ккал, а при образовании иона [ AgH201 41 5 ккал. Если не принимать во внимание поляризации, то гидрат должен был бы быть прочнее. Если учитывать только заряд и перманентный диполь NH3 и не принимать во внимание поляризуемости Ag, то при образовании иона [ AgNH3 ] должно выделиться всего 40 ккал. Разумеется, если ион типа инертного газа обладает благоприятным соотношением заряда и радиуса, то его поляризующее действие может достигнуть столь больших размеров, что он все-таки будет давать аммиакаты в водном растворе. [10]
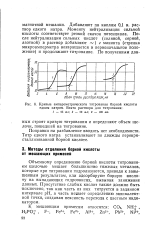 |
Кривые амперометрического титрования борной кислоты едким натром. Взято раствора для титрования. [11] |
Объемному определению борной кислоты титрованием щелочью мешает большинство тяжелых металлов, которые при титровании гидролизуются, приводя к завышенным результатам, или адсорбируют борную кислоту на выпадающих гидроокисях, вызывая занижение данных. Присутствие слабых кислот также должно быть исключено, так как часть из них титруется в заданном интервале рН, а часть мешает определению эквивалентной точки, создавая неясность перехода с цветным индикатором. [12]
Восстанавливает также сульфиды, га-логениды и цианиды большинства тяжелых металлов. [13]
Попадая в организм, свинец, как и большинство тяжелых металлов, вызывает отравления. И тем не менее свинец нужен медицине. Со времен древних греков остались во врачебной практике свинцовые примочки и пластыри, но этим не ограничивается медицинская служба свинца. [14]
Его можно предварительно отделить ( а также и большинство тяжелых металлов) указанной выше обработкой суспензией гидроокиси алюминия. [15]
Страницы: 1 2 3 4