Большинство - реактив
Cтраница 2
Стеклянная посуда и аппаратура находят широкое применение в лабораториях, так как они устойчивы к действию большинства реактивов, довольно дешевы и их легко мыть. Кроме того, прозрачность стекла дает возможность наблюдать за реакцией не только посредством измерительных приборов, но и путем визуальной оценки внешнего вида реакционной массы. Все это способствует внедрению стеклянных изделий в лабораторную практику, хотя недостаточная механическая прочность и неустойчивость обычных сортов стекла к резким изменениям температуры нередко приводят к поломке стеклянных изделий, что является причиной многих ранений в лабораториях. [16]
Этот реактив Рейнольде и Юм-Розери [39] рекомендовали для сплавов алюминий - кремний ( литье в песчаные формы и кокильное литье с содержанием 5, 10 и 11 % кремния в немодифицированном и модифицированном состояниях), так как большинство реактивов растворяют толькд алюминиевый твердый раствор как основную структуру без всякого контрастного различия. [17]
В заключение параграфа несколько слов о кислотности растворов. Большинство реактивов капельного анализа представ - - ляет собой слабые органические основания или кислоты ( или их соли), которые чрезвычайно чутко реагируют на любую степень изменения кислотности или щелочности. [18]
 |
Реактивная склянка с пипеткой ( 2 - й образец. [19] |
Студенты работают быстрее, чище и точнее, чем при макрометоде. Большинств реактивов находится на рабочем месте, за ними не нужно ходить, что способствует более сосредоточенной и обдуманной работе. Все это заметно улучшает химическую подготовку студента. [20]
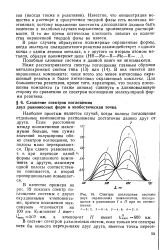 |
Спектры поглощения системы двух окрашенных компонентов, находящихся в равновесии / и / / при их соотношении. [21] |
В них имеется два окрашенных компонента: чаще всего это менее интенсивно окрашенный реактив и более интенсивно окрашенный комплекс. Для большинства реактивов, кроме того, характерно, что полоса поглощения комплекса ( а также аниона) сдвинута в длинноволновую сторону по сравнению со спектром поглощения молекулярной формы реактива. [22]
Кроме указанных ниже реактивов, для никеля можно применять способы травления, приведенные для никелевых сталей. С помощью большинства реактивов у никеля выявляют только границы зерен вследствие плохой окисляемости. [23]
Кристаллы камфары обладают значительной летучестью, легко слеживаются в сплошной конгломерат, а под небольшим давлением превращаются в прозрачную глыбу. Камфара реагирует с большинством реактивов, применяемых для идентификации кетонов. С бисульфатом натрия не реагирует. Эти спирты различаются лишь пространственным расположением атомов Н и ОН при втором С-атоме: у борнеола группа ОН направлена внутрь кольца, а у изоборнеола - наружу. На плоскости оба спирта изображаются одной и той же формулой. [24]
Реакции с дитизоном чрезвычайно чувствительны и нередко превышают в этом отношении чувствительность спектрального анализа. Столь большая чувствительность реакции создает даже некоторые трудности применения дитизона, так как с помощью его обнаруживаются примеси тяжелых металлов в большинстве реактивов и даже в однократно перегнанной дестиллированной воде. Дитизон нерастворим в воде, но растворим в щелочах с образованием солей. Для анализа применяют растворы самого реактива и его соединений с металлами в СНС13 или ССЦ, причем раствор дитизона окрашен в интенсивно зеленый цвет. [25]
В опытах, описанных в книге, как правило, применяются малые количества веществ ( жидкости - от одной капли до 1 - 2 мл, сухие вещества - 0 05 - 1 0 г), поэтому большинство реактивов сохраняется в флаконах из-под пенициллина, укрепленных в штативах-колодках. [26]
Значительное уменьшение объемов стеклянной химической посуды создает возможности для ее компактного размещения на рабочем столе при проведении опытов. Работа выполняется быстрее и точнее, чем макрометодом. Большинство реактивов можно держать на рабочем месте, что способствует более сосредоточенной и обдуманной работе. [27]
Следует иметь в виду, что при проведении подготовительных операций и приготовлении растворов сравнения ( в особенности при их длительном хранении) возможны заметные потери этих элементов; при определении малых концентраций это приводит к большим ошибкам. Потери серебра происходят обычно из-за его выпадения в осадок в виде малорастворимого хлорида. Предотвратить их нелегко, так как большинство реактивов, а часто и дистиллированная вода, содержат примесь хлорид-иона. [28]
Образующиеся при этом кетоны обычно значительно реакционно-способнее сложных эфиров, так что реакция не останавливается на стадии образования кетона, а идет дальше, давая в результате третичный спирт, часто с хорошим выходом. Для получения кетонов из сложных эфиров можно использовать метод обратного прибавления реагентов, при этом металлоорганическое соединение помещают в капельную воронку и медленно добавляют к эфиру, что обеспечивает постоянный избыток эфира по сравнению с кетоном; но даже при этом обычно образуется некоторое количество третичного спирта. В результате пространственных затруднений во второй стадии реакции большинство реактивов Гриньяра с хорошим выходом образует кетоны. [29]
Если не были приняты специальные меры, то при обычном ходе анализа горных пород часть олова улетучится, а часть выпадет в осадок вследствие гидролиза и выделится вместе с кремнекислотой. Продукты гидролиза солей олова, присоединяясь к осадку кремнекислоты, могут быть причиной ошибки в определении кремния, так как они изменяют свой состав, когда нечистая кремнекислота обрабатывается фтористоводородной и серной кислотами и остаток примесей прокаливается. В обычном ходе анализа горных пород та часть олова, которая не улетучится при выпаривании с соляной кислотой, попадет в осадок от аммиака и будет принята за алюминий, потому что большинство реактивов, применяемых для восстановления железа, не восстанавливает олова. Цинк, являющийся исключением, обычно восстанавливает все олово в редукторе Джонса до металла. Таким образом и при применении цинка для восстановления железа олово не оказывает влияния на титрование железа, если только оно не перейдет в раствор до конца титрования. [30]
Страницы: 1 2 3