Большинство - химическая реакция
Cтраница 3
Большинство химических реакций требует энергии активации, т.е. преодоления определенного энергетического барьера. В связи с этим они находятся под кинетическим контролем. Когда образуется продукт реакции определенной толщины, то для продолжения процесса наиболее подвижные компоненты должны преодолевать диффузионное сопротивление слоя этих продуктов. [31]
Большинство химических реакций являются обратимыми. [32]
Большинство химических реакций являются обратимыми. [33]
Большинство химических реакций не протекает до конца. Реакции, которые могут одновременно протекать в прямом и обратном направлениях, называются обратимыми. [34]
 |
Изменение скорости прямой ( 7 и обратной ( 2 реакций с течением времени. [35] |
Большинство химических реакций являются обратимыми. [36]
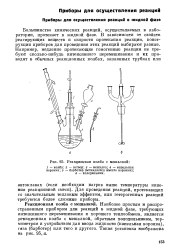 |
Реакционная колба с мешалкой. [37] |
Большинство химических реакций, осуществляемых в лаборатории, протекает в жидкой фазе. В зависимости от свойств реагирующих веществ и скорости протекания реакции, конструкции приборов для проведения этих реакций выбирают разные. [38]
 |
Изменение скорости прямой ( I и обратной ( 2 реакций с течением времени. [39] |
Большинство химических реакций являются обратимыми. [40]
Большинство химических реакций протекает в виде последовательности промежуточных стадий, поэтому полное описание может включать расчет концентраций нескольких десятков компонентов. [41]
 |
Изменение скорости прямой ( I и обратной ( 2 реакций с течением времени. [42] |
Большинство химических реакций являются обратимыми. [43]
Большинство химических реакций не протекает до конца. Реакции, которые могут одновременно протекать в прямом и обратном направлениях, называются обратимыми. [44]
Большинство химических реакций является процессами обратимыми. Это значит, что они не доходят до конца, а в известный момент в них устанавливается равновесие, при котором вещество, образующееся в ходе реакции, с такой же скоростью подвергается разложению. Химическое равновесие обычно сильно зависит от температуры. [45]
Страницы: 1 2 3 4