Большинство - вещество
Cтраница 2
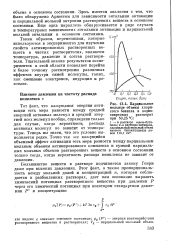 |
Парциальные мольные объемы хлористого бензила в водно-спиртовых растворах при 50 25. С. [16] |
Большинство веществ в растворе подчиняется закону Генри даже при высоких давлениях. [17]
Большинство веществ, обнаруживающих люминесценцию, содержат примеси, и у чистых веществ это явление весьма редко наблюдается. [18]
Большинство веществ способно вступать в многочисленные химические реакции. Рассмотрению этих реакций придается важное значение при изучении химии. [19]
Большинство веществ, построенных из ионов с оболочками типа инертного газа, бесцветны и окрашенными оказываются только в том случае, если они содержат электроположительные атомы с особенно сильными поляризационными свойствами. Так, сложные ионы СгО - и МпО - окрашены, хотя они ( поскольку связи в них рассматриваются как гетеро-полярные) и построены из ионов с оболочками типа инертных газов. Так как способность к поляризации возрастает с увеличением заряда и падает с увеличением ионного радиуса, то ионам или атомным остовам Сг6 и Мп7, характеризующимся высоким зарядом и одновременно малым радиусом, следует приписать особенно сильную поляризационную способность. [20]
Большинство веществ, построенных из ионов с оболочками типа инертного газа, бесцветны и окрашенными оказываются только в том случае, если они содержат электроположительные атомы с особенно сильными поляризационными двойствами. Так, сложные ионы СгО - и МпО - окрашены, хотя они ( поскольку связи в них рассматриваются как гетеро-полярные) и построены из ионов с оболочками типа инертных газов. Так как способность к поляризации возрастает с увеличением заряда и падает с увеличением ионного радиуса, то ионам или атомным остовам Сг6 и Мп % характеризующимся высоким зарядом и одновременно малым радиусом, следует приписать особенно сильную поляризационную способность. [21]
Большинство веществ сильно поглощает вблизи 200 нм, но прозрачно для случайного света. Это приводит к появлению в коротковолновой области ложных максимумов, обусловленных пропусканием и регистрацией случайного света. При данной длине волны ошибка, вызываемая таким излучением, увеличивается тем значительнее, чем сильнее поглощает растворитель. [22]
Большинство веществ может находиться только в трех агрегатных состояниях: твердом, жидком или газообразном. Однако некоторые органические вещества, обладающие сложными молекулами, могут образовывать четвертое, жидкокристаллическое. Как следует из самого названия, речь идет о специфическом агрегатном состоянии вещества, в котором оно проявляет одновременно свойства кристалла и жидкости. Оказывается, что при плавлении кристаллов этих веществ образуется жидкокристаллическая фаза, отличающаяся от обычных жидкостей. Эта фаза существует в интервале от температуры плавления до некоторой более высокой температуры, при нагреве до которой жидкий кристалл переходит в обычную жидкость. [23]
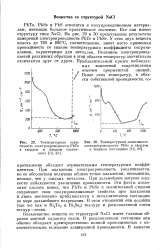 |
Температурная зависимость. [24] |
Большинство веществ со структурой NaCl имеет главным образом ионный характер связи. В расплавленном состоянии они обычно обладают преимущественно ионной проводимостью с незначительными следами электронной проводимости. [25]
Большинство веществ является правовращающими. Такие вещества называют положительными. К ним относятся все диамагнетики. Имеются и отрицательные вещества, которые обязательно содержат парамагнитные атомы. [26]
Большинство веществ при сублимации ведет себя сложно: и просто испаряются, и одновременно диссоциируют. При этом в газообразной фазе находится смесь целых молекул и их обломков. Нельзя точно сказать, какая же доля фазы приходится на целые молекулы, а какая на их осколки. А для процесса фракционного осаждения знать это просто обязательно. [27]
Большинство веществ способно вступать в многочисленные химические реакции. Рассмотрению этих реакций придается важное значение при изучении химии. Химию можно определить как науку о веществах - об их строении, свойствах и о реакциях, в результате которых одни вещества превращаются в другие. [28]
Большинство веществ ( главным образом соли), обладающих в растворе свойствами сильных электролитов, образуют - в чистом состоянии ионные кристаллы или расплавы. Растворение этих так называемых истинных электролитов - не что иное, как распад на ионы под влиянием молекул - - растворителя. Ионы в кристалле удерживаются кулоновскими силами. В растворах, обычно определяемых как идеальные электролиты, преобладает электростатическое взаимодействие ионов и в небольшой степени могут образовываться ионные пары. Ковалентные молекулы, как правило, не образуются. Однако в растворителях с низкой диэлектрической проницаемостью ионная ассоциация заметна даже в разбавленных растворах. [29]
Большинство веществ в чистом виде обладают определенной температурой плавления, ниже которой происходит переход от статистической структуры жидкости к высокоупорядоченной периодической кристаллической структуре. [30]
Страницы: 1 2 3 4