Большинство - элемент
Cтраница 3
 |
Некоторые гидридные соединения переходных металлов. [31] |
Большинство элементов, вошедших в табл. 8.3, образует карбонилгидриды, часто кластерного строения, причем атомы водорода в них играют роль мостиков между двумя и тремя атомами металла. В некоторых кластерах металлов атом водорода занимает положение в пустотах, например в HNbeln ( разд. Структуры карбонилов металлов рассмотрены в гл. [32]
Большинство элементов образует соединения с элементным азотом, и среди нитридов имеется целый ряд очень устойчивых соединений. [33]
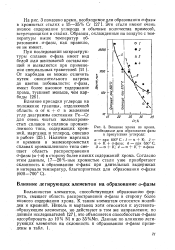 |
Влияние хрома на время. [34] |
Большинство элементов, способствующих образованию феррита, смещает область распространения а-фазы в сторону более низкого содержания хрома. К таким элементам относятся молибден и кремний. Никель и марганец хотя относятся к аустенйто-образующим элементам, но действуют в том же направлении; по данным исследователей [27], это объясняется способностью 0-фазы адсорбировать до 10 % Ni и до 35 % Мп. [35]
Большинство элементов, содержащихся в природе, состоит из нескольких видов атомов, отличающихся значениями относительной атомной массы. [36]
Большинство элементов имеет несколько изотопов. [37]
Большинство элементов третьей группы также образует прочные соединения с фтором. Таким образом, фтор образует комплексы с широким кругом элементов, преимущественно центра таблицы Менделеева. Однако, это не означает, что ион фтора вовсе не реагирует с ионами типичных металлов комплекеообразо-вателей, имеющими недостроенную d - оболочку. Так, железо ( III) при реакции с ионом фтора проявляет ряд аналогий с алюминием. В отличие от большинства соединений железа его фторидные комплексы бесцветны. [38]
 |
Природное содержание изотопов в некоторых элементах. [39] |
Большинство элементов представляет собой смесь различных изотопов, относительное природное содержание которых является довольно постоянной величиной. Этот факт отражается в масс-спектре двояким образом. Во-первых, даже очень чистое соединение дает для молекулярного иона не один, а ряд пиков, отвечающих каждой из возможных комбинаций изотопов присутствующих атомов. [40]
Большинство элементов в кислой среде не осаждается бензол-или нафталинселенинатом аммония и не мешает определению циркония, за исключением Sn ( IV), Ti ( IV), Nb ( V) и Ta ( V), образующих в кислых растворах аналогичные осадки. Влияние последних трех элементов устраняют прибавлением перекиси водорода. Олово должно быть предварительно удалено осаждением сероводородом. [41]
Большинство элементов, как известно, представлено несколькими стабильными изотопами, поэтому их атомная масса выражается дробными числами. Можно было бы предположить, что значение атомной массы хлора должно быть где-то между 35 и 37 с учетом распространенности в природе атомов хлора-35 и хлора-37. [42]
Большинство элементов имеет несколько изотопов. [43]
Большинство элементов в таблице содержится внутри фигурных скобок, которые указывают на отражение относительно наиболее удаленных от середины разрядов. [44]
Большинство элементов имеет по нескольку настолько устойчивых изотопов, что они существуют в природных условиях на земле. Интересное и многозначительное обстоятельство-это то, что все массовые числа приведенных изотопов, указанные наверху справа, нечетны; далее, за исключением бериллия, также нечетны числа протонов, указанные внизу слева у символов элементов. В течение последнего десятилетия эта особенность была объяснена, исходя из модели атомного ядра, имеющей оболочечную структуру, в какой-то степени напоминающую оболочеч-ную структуру и периодичность самих атомов. [45]
Страницы: 1 2 3 4