Подавляющее большинство - металл
Cтраница 2
Подавляющее большинство металлов кристаллизуется в одном или нескольких из трех типов структур. В кристаллохимии для этих структурных типов используют обозначения Al, A2 и A3, соответственно. Лишь небольшое число металлов имеет более сложное строение. Сложной кристаллической структурой обладают также интерметаллические соединения. [16]
 |
Виды местной коррозии металла. [17] |
Подавляющее большинство металлов в земной коре находится в связанном состоянии в виде окислов, солей и других соединений. Причина этого явления состоит в термодинамической неустойчивости металлов. [18]
Подавляющее большинство металлов ( за исключением щелочных и некоторых щелочноземельных, имеющих очень отрицательные значения электрохимических потенциалов) осаждаются из растворов своих солей под действием постоянного электрического тока. Взаимосвязь между количествами пропущенного чгрез раствор электричества и выделившегося металла определяется законами Фарадея и практически сводится к тону, что для выделения одного граммэквивалента любого металла затрачивает Ъ 26 8 анперчаса. Однако, в большинстве случаев, количество выделившегося при электролизе металла не соответствует количеству пропущенного через раствор электричества, а бывает несколько или значительно меньше. [19]
Подавляющее большинство металлов и сплавов уменьшается в объеме при переходе из жидкого в твердое состояние. Исключение составляет важнейший литейный сплав - серый чугун, практически не имеющий объемной усадки, так как у него уменьшение объема при кристаллизации компенсируется увеличением объема из-за выделения в структуре свободного графита. [20]
 |
Образование энергетических зон в металлических кристаллах из атомных электронных уровней ( d - расстояние между атомами, d0 - расстояние между ними в кристалле. [21] |
Подавляющее большинство металлов кристаллизуется в наиболее плотных структурах - в плотнейшей кубической ( гранецентри-рованной), плотнейшей гексагональной, несколько реже - в кубической объемно-центрированной. В табл. 14 приведены кристаллические структуры, свойственные некоторым металлам. [22]
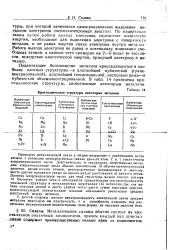 |
Кристаллические структуры некоторых металлов. [23] |
Подавляющее большинство металлов кристаллизуется в наиболее плотных структурах-в плотнейшей кубической ( гране-центрированной), плотнейшей гексагональной, несколько реже-в кубической объемноцентрированной. В табл. 14 приведены кристаллические структуры, свойственные некоторым металлам. [24]
Подавляющее большинство металлов кристаллизуется в наиболее плотных структурах - в плотнеишеи кубической ( гранецентри-рованной), плотнеишеи гексагональной, несколько реже в кубической объемно-центрированной. В табл. 36 приведены кристаллические структуры, свойственные некоторым металлам. [26]
Подавляющее большинство металлов соединяется с фтором уже при обычных условиях. Однако взаимодействие часто ограничивается образованием плотной поверхностной пленки фтористого соединения, которая предохраняет металл от дальнейшего разъедания. [27]
Подавляющее большинство металлов соединяется с фтором уже при обычных условиях, взаимодействие его с неметаллами протекает еще энергичнее, чем с металлами. Химическая активность падает в ряду F - - С1 - Вг - I, но все же остается достаточно большой даже для иода. Многие галогениды металлов получают обменными реакциями в растворах. [28]
Подавляющее большинство металлов соединяется с фтором уже при обычных условиях. Однако взаимодействие часто ограничивается образованием плотной поверхностной пленки фтористого соединения, которая предохраняет металл от дальнейшего разъедания. [29]
Подавляющее большинство металлов соединяется с фтором уже при обычных условиях. Однако взаимодействие часто ограничивается образованием поверхностной пленки фтористого соединения, которая предохраняет металл от дальнейшего разъ-единения. [30]
Страницы: 1 2 3 4
