Подавляющее большинство - химический процесс
Cтраница 1
Подавляющее большинство химических процессов в живой природе - окислительно-восстановительные реакции, и непременное условие таких реакций - обмен электронами. Здесь всегда взаимодействуют как минимум два партнера, один из которых принимает электроны ( окислитель), а другой их отдает. Конечно, при этом меняются и сами молекулы, они распадаются или из них, наоборот, строятся новые, более крупные, но суть большинства этих превращений - обмен электронами. Основной биохимический процесс, дыхание, без которого невозможна жизнь на Земле - тоже окислительно-восстановительная реакция. [1]
Для подавляющего большинства химических процессов уменьшение степени превращения, достигаемое на конце реактора за счет смягчения жесткости режима, приводит к одновременному увеличению мощности установки по сырью и по целевому продукту. [2]
Для подавляющего большинства химических процессов, в том числе и для синтеза аммиака, важно, чтобы скорость реакции была достаточно велика. [3]
В подавляющем большинстве химических процессов - реакциях обмена - одна составляющая часть вещества вытесняет другую не только благодаря большей силе своего сродства но я благодаря большей массе, взятой в реакцию. [4]
Мы уже указывали, что подавляющее большинство химических процессов протекает в растворах. Например, два твердых вещества могут практически не вступать в реакцию друг с другом, и вместе с тем растворы этих веществ способны быстро реагировать. Так происходит с порошкообразной смесью твердого NaHCO3 и твердой кислоты NaH2PO4 ( или квасцов); эта смесь используется в хлебопекарной промышленности. [5]
При таком более широком рассмотрении подавляющее большинство химических процессов оказывается принадлежащим к типу обратимых, но часто с настолько смещенным в одну сторону равновесием, что их обратимость практически незаметна до тех пор, пока соответственно не изменятся внешние условия. Именно эта распространенность обратимых реакций обусловливает особую важность для химии изучения равновесий и условий их смещения. [6]
При таком более широком рассмотрении подавляющее большинство химических процессов оказывается принадлежащим к типу обратимых, но часто с настолько смещенным в одну сторону равновесием, что их обратимость практически незаметна до тех пор, пока соответственно не изменяются внешние условия. Именно эта распространенность обратимых реакций обусловливает особую важность для химии изучения равновесий и условий их смещения. [7]
При таком более широком рассмотрении подавляющее большинство химических процессов оказывается принадлежащим к типу обратимых, но часто с настолько смешимым в одну сторону равновесием, что их обратимость практически незаметна до тех пор, пока соответственно не изменятся внешние условия. [8]
 |
Стандартные изобарные потенциалы некоторых веществ. [9] |
Необходимо помнить, что температура, при которой происходит подавляющее большинство химических процессов, значительно выше 25 С, и поэтому экстраполировать результаты расчета на высокие температуры следует с известной осторожностью. Часть реакций синтеза веществ при стандартных условиях является гипотетической. Это, однако, не может служить препятствием к расчету AZ s, так как изменение изобарного потенциала не зависит от пути перехода. [10]
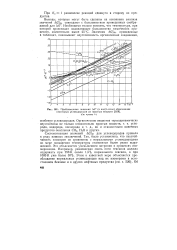 |
Приближенные значения ДС ( в кал / г-атом образования. [11] |
Необходимо только помнить, что температура, при которой происходит подавляющее большинство химических процессов, значительно выше 25 С. [12]
Воздушное и газовое хозяйство современного химического завода очень велико, так как подавляющее большинство химических процессов связано с необходимостью подачи и отвода газов и воздуха, что влечет за собой необходимость их сжатия при помощи воздухо - и газодувных машин. [13]
В настоящее время нахождение оптимальных значений параметров, основанное на математическом моделировании, для подавляющего большинства химических процессов невыполнимо ввиду отсутствия достаточно полного математического описания отдельных аппаратов, узлов и всего производства в целом. Поэтому выбор оптимальных значений параметров на основе математического моделирования производят только для наиболее важных физических и химических операций; остальные же операции оформляются пока на основе обычных инженерных расчетов с выбором значений параметров по результатам лабораторных и опытных работ, анализа показателей работы действующих производств и инженерной интуиции. Достаточно полные математические описания составлены в настоящее время только для некоторых наиболее простых и хорошо изученных технологических процессов. [14]
В дальнейшем, если это особо не оговорено, уравнения ( 11 3) и ( П 4) будут применяться исключительно в виде ( 11 5) или ( 11 6), так как подавляющее большинство химических процессов протекает при постоянном внешнем давлении в отсутствие каких-либо других воздействий на систему. [15]
Страницы: 1 2