Подавляющее большинство - соединение
Cтраница 1
Подавляющее большинство соединений, содержащих кратную связь ( двойную, тройную, их комбинации, за исключением ароматических систем), легко присоединяют бром. [1]
Подавляющее большинство соединений х - и р-элементов ( в отличие от соединений ( / - элементов) бесцветно, так как исключен обусловливающий окраску переход ( / - электронов с низких энергетических уровней на более высокие по энергии. Окраска некоторых соединений s - н р-элементов объясняется не эффектами кристаллического поля, а другими причинами. Такие окрашенные соединения, как PbS - черный, РЫг-желтый, SbzSs - оранжевый, содержат сильно поляризуемые ионы, поляризация вызывает расщепление энергетических уровней s - и р-электронов, что аналогично воздействию кристаллического поля на ( / - электроны. Следует отметить, что окрашенные вещества составляют лишь небольшую долю от общего числа соединений s - и р-элементов. [2]
Подавляющее большинство соединений, содержащих силокса-новые связи ( кроме силанолов), в растворах неполярных растворителей мало склонно к аутоассоциации или к донорно-акцепторно-му взаимодействию с растворителем. Об этом свидетельствуют весьма многочисленные результаты определения молекулярных весов и данные других физико-химических исследований. [3]
Подавляющее большинство соединений х - и р-элементов ( в отличие от соединений ( / - элементов) бесцветно, так как исключен обусловливающий окраску переход ( / - электронов с низких энергетических уровней на более высокие по энергии. Окраска некоторых соединений s и р-элемеитов объясняется не эффектами кристаллического поля, а другими причинами Такие окрашенные соединения, как PbS - черный, РЬ2 - желтый, SbjSj-оранжевый, содержат сильно поляризуемые ионы, поляризация вызывает расщепление энергетических уровней I - и р-электронов, что аналогично воздействию кристаллического поля на ( / - электроны. Следует отметить, что окрашенные вещества составляют лишь небольшую долю от общего числа соединений - и р-элементов. [4]
Подавляющее большинство соединений, представляюших биологический интерес, содержат не только каталитически актив-лую серу, но и азот в виде аминогрупп, также обладающий способностью катализировать выделение водорода. Наблюдаемый в растворах таких соединений каталитический эффект определяется общим действием всех активных групп в молекуле. Сунахара [795] на примере волн, вызываемых цистином и его производными, в которых блокированы либо аминогруппы - диацетилцистин), либо карбоксилы ( диэтиловый эфир цистина), показал, что блокирование аминогрупп приводит к полной потере каталитической активности цистина, тогда как этерификация карбоксилов почти не сказываегся на каталитической волне. [5]
Подавляющее большинство соединений, представляюших биологический интерес, содержат не только каталитически активную серу, но и азот в виде аминогрупп, также обладающий способностью катализировать выделение водорода. Наблюдаемый в растворах таких соединений каталитический эффект определяется общим действием всех активных групп в молекуле. Сунахара [795] на примере волн, вызываемых цистином и его производными, в которых блокированы либо аминогруппы - диацетилцистин), либо карбоксилы ( диэтиловый эфир цистина), показал, что блокирование аминогрупп приводит к полной потере каталитической активности цистина, тогда как этерификация карбоксилов почти не сказывается на каталитической волне. [6]
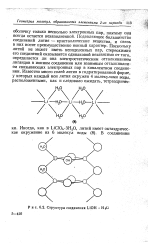 |
Структура соединения LiOH. [7] |
Подавляющее большинство соединений лития - кристаллические вещества, и связь в них носит преимущественно ионный характер. Поскольку литий не может иметь неподеленных пар, стереохимия его соединений оказывается одинаковой независимо от того, определяется ли она электростатическим отталкиванием лигандов в ионном соединении или взаимным отталкиванием связывающих электронных пар в ковалентном соединении. [8]
 |
Кристаллические структуры типа сфалерита ( и и вюрцита ( б. [9] |
Подавляющее большинство соединений AnlBv кристаллизуется в решетке цинковой обманки либо кубического ( сфалерит), либо гексагонального ( вюрцит) типа. Для решеток обоих типов характерна тетрагональная координация атомов. Структура сфалерита может рассматриваться как комбинация двух вставленных одна в другую кубических гранецентрированных решеток, смещенных относительно друг друга на четверть диагонали куба и состоящих из одного сорта атомов каждая. [10]
Подавляющее большинство соединений органической химии способно давать множество самых различных гомологических рядов. За счет этого достигается исключительное богатство органических соединений. [11]
В подавляющем большинстве соединений средняя длина связи Сг - С ( Со) лежит в пределах 1 82 - 1 85 А. Это расстояние значительно короче найденного в Сг ( СО) 6 ( 1 92 А) и близко к обнаруженным в октаэдрах в транс-положении к кар-беновому углероду. Однако этой особенности вряд ли можно придавать большое значение, поскольку оба расстояния определяются координатами атома углерода, точность оценки которых относительно низка. [12]
В подавляющем большинстве соединений атомы кислорода поляризованы отрицательно. Положительная поляризация наблюдается в соединениях с фтором. [13]
В подавляющем большинстве соединений углерод четырехвалентен. Соединения углерода с незаполненными орбитами, а именно с семью электронами ( свободные радикалы), неустойчивы. Соединения с атомом углерода, связанным с двумя другими одновалентными атомами, обладающие, таким образом, шестью электронами у атома углерода, как, например, метилен СН2, тоже неустойчивы. В этом отношении они похожи на свободные радикалы. Тем более удивительным является тот факт, что окись углерода СО - очень устойчивое вещество, обладающее неожиданной инертностью в химических реакциях. [14]
В подавляющем большинстве соединений углерод четырехвалентен. Соединения углерода с незаполненными орбитами, а именно с семью электронами ( свободные радикалы), неустойчивы. Соединения с атомом углерода, связанным с двумя другими одновалентными атомами, обладающие, таким образом, шестью электронами у атома углерода, как, например, метилен СНа, тоже неустойчивы. В этом отношении они похожи на свободные радикалы. Тем более удивительным является тот факт, что окись углерода СО - очень устойчивое вещество, обладающее неожиданной инертностью в химических реакциях. [15]
Страницы: 1 2 3 4