Перезащита
Cтраница 1
Перезащита может быть вызвана не только амфотерным характером металлов, но и образованием гидридов металлов, что впол -, не вероятно при высокой плотности тока и интенсивном выделении водорода на катодно защищаемом металле. Явление перезащиты отмечено для алюминия и свинца. [1]
Умеренная перезащита стальной конструкции обычно не приносит вреда. Основными недостатками при этом являются потери электроэнергии и возрастающий расход вспомогательных анодов. При сильной перезащищенности возникает дополнительный ущерб в случае, если на защищаемой поверхности выделяется так много водорода, что это вызывает либо вспучивание или отслаивание органических покрытий, либо водородное охрупчивание стали ( потерю пластичности в результате абсорбции водорода), либо растрескивание под действием водорода ( см. разд. Разрушение стали в результате абсорбции водорода, по существу, близко к разрушениям, происходящим в сульфидсодержащих средах [20] ( см. разд. [2]
Небольшая перезащита стальных сооружений обычно не причиняет ущерба. Основные неудобства в этом случае связаны с потерей электрической энергии и повышенным износом вспомогательных анодов. [3]
Явление перезащиты при катодной поляризации стали 5 проследить довольно трудно, так как эффект небольшой. Оно выражается лишь некоторым уменьшением степени защиты стали при значительных увеличениях отношения внешнего тока к коррозионному. [4]
Режим перезащиты вообще недопустим при защите кабелей в свинцовых и алюминиевых оболочках. Такой характер изменения потенциалов газопроводов и других подземных металлических сооружений приводит к необходимости создания автоматических устройств катодной защиты, которые должны поддерживать потенциал в защитном диапазоне при минимальном расходе электроэнергии и максимальном использовании защитных свойств блуждающих токов. При применении автоматических дренажей уменьшение расхода электроэнергии в сравнении с неавтоматическими усиленными дренажами помимо энергетических преимуществ снижает опасность разрушения рельсов электрифицированных железных дорог. [5]
В случаях перезащиты амфотерных металлов ( например, А1, Zn, Pb, Sn) образующийся при этом избыток щелочи вызывает разрушение металла большее, чем снижение коррозии из-за катодной защиты. Для свинца было показано [16], что катодная защита возможна и в щелочном диапазоне рН, однако потенциал, при котором достигается полная защита, сдвигается при этом в сторону более отрицательных значений. [6]
Наиболее ярко выражено явление перезащиты для таких металлов, как свинец и алюминий. Окислы этих металлов оказываются хорошо растворимы и в кислотах, и в щелочах. Окислы алюминия легко растворяются в щелочи с образованием алюминатов. Зависимость скорости растворения алюминия от плотности тока и потенциала приведена в табл. 45, а в табл. 46 и 47 сведены данные по катодной коррозии свинца в растворах хлористого калия ( различной концентрации) и в 0 1 н растворе NaOH. В последней таблице показано снижение скорости коррозии и последующее ее возрастание при высоких отрицательных потенциалах. [7]
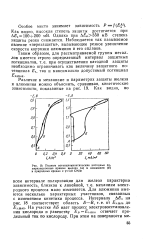 |
Полные потенциокинетические катодные поляризационные кривые железа ( а н алюминия ( б в природных средах с v3 0 СМ / м. [8] |
Наблюдается так называемое явление перезащиты, вызывающее резкое увеличение скорости коррозии алюминия и его сплавов. [9]
Степень зашиты, включая перезащиту, определяют, измеряя потенциал защищаемого сооружения. Эти измерения имеют большое значение для практики и широко используются инженерами-коррозионистами. Сущность этого метода основана на представлении, что полностью катодная защита достигается в том случае, когда защищаемое сооружение поляризовано до обратимого потенциала анодных участков локальных пар. Для стали величина этого потенциала, определенная эмпирическим путем, составляет - 0 85 в по отношению к насыщенному медно-сульфатному электроду, или - 0 53 в по стандартной водородной шкале. [10]
Исследование водородного разрушения при перезащите [109] показало, что присутствие кислорода в коррозионной среде тормозит наводороживание и, соответственно, наступление хрупкого разрушения. [11]
Исследование водородного разрушения при перезащите [109] показало, что присутствие кислорода в коррозионной среде тормозит наводороживание и, соответственно, наступление хрупкого разрушения. [12]
Однако в этом случае опасна перезащита - возможность сдвига потенциала положительнее Фпер, когда начинается процесс перепассивации. [13]
При катодной защите оборудования следует избегать перезащиты, так как она вызывает отслаивание лакокрасочных покрытий и водородную хрупкость высокопрочных сталей. [14]
Критерий степени защиты, включая и перезащиту, получают с помощью измерения потенциала защищаемой конструкции. Для практики эти измерения наиболее важны, они общеприняты и широко используются специалистами по коррозии. Такой подход основан на фундаментальном положении, что оптимум катодной защиты достигается, когда защищаемая конструкция поляризована до потенциала анодных участков в отсутствие тока. Этот эмпирически установленный потенциал для стали равен - 0 85 В по отношению к насыщенному медносульфатному электроду или - 0 53 В. [15]
Страницы: 1 2 3 4