Перекрытие - электронное облако
Cтраница 1
Перекрытие электронных облаков между атомами весьма быстро изменяется при изменении расстояния между ядрами. Это означает, что силы ковалентнои связи обычно велики. Поэтому ковалентные кристаллы, как правило, очень твердые и имеют высокие температуры плавления. Типичным ковалентным кристаллом является, например, алмаз. [1]
Перекрытие электронных облаков, приводящее к обобществлению электронов, не сводится к простому наложению друг на друга двух сферически симметричных электронных облаков изолированных атомов, а сопровождается существенным перераспределением электронной плотности и изменением энергии системы. При обобществлении электронов происходит втягивание электронных облаков в пространство между ядрами атомов: в пространстве между ядрами плотность электронного облака будет больше, чем должна была бы получиться плотность облака при простом сложении двух электронных облаков изолированных-атомов, в то же время на небольшом расстоянии от ядер вне этого пространства плотность электронного облака становится меньше, чем в изолированных атомах. Штриховая линия / показывает плотность электронных облаков изолированных атомов, пунктирная линия 2 показывает суммарную плотность, которая получилась бы при простом наложении электронных облаков двух изолированных атомов, сближенных до расстояния г, на участках /, 2 кривые 1 и 2 практически сливаются. Сплошная жирная кривая 3 показывает распределение плотности электронного облака в молекуле водорода вдоль оси, соединяющей ядра атомов. [2]
 |
Гибридизация s -, р-электрон-ных облаков. [3] |
При перекрытии электронных облаков область наибольшей плотности заряда может расположиться вдоль линии центров ( прямой, соединяющей центры атомов) или вне ее. [4]
В случае промежуточных г, когда перекрытие электронных облаков пренебрежимо мало, некоторые важные члены, дающие вклад в FYe ( r) имеют более тонкое происхождение. Для подробных вычислений здесь также необходима квантовомеханиче-ская теория возмущений. Однако теперь роль возмущения играет оператор Я, соответствующий взаимодействию между различными зарядовыми мультиполями, одновременно имеющимися у каждого иона. [5]
Силы, действующие между полярными молекулами, как и между неполярными, делятся на силы отталкивания, вызываемые перекрытием электронных облаков, и лондоновские дисперсионные силы притяжения. В дополяение к этому следует отметить, что полярность определяется постоянным несимметричным распределением заряда, которое приводит к появлению электростатической составляющей потенциальной энергии. Обычно составляющую потенциальной энергии выражают в виде бесконечного ряда обратных степеней межмолекулярного расстояния. [6]
Связь образуется двумя облаками электронов, лежащими в одной плоскости, перпендикулярной к плоскости молекулы, в отличие от а-связей, где перекрытие электронных облаков полное. Облака я-электронов в л-свя-зи только частично перекрываются. В силу этих причин двойная связь является химически реакционноопособной; за счет реакций присоединения и полимеризации она легко переходит в простую связь. В реакции полимеризации могут участвовать соединения с двойными связями между атомами углерода С С, углерода и кислорода С О, углерода и азота С N - и пр. Соединения с тройными - СС - связями полимеризуются легче олефинов. [7]
Если такое распределение сохраняется для каждого иона, независимо от его положения, из электростатики будет следовать, на основе теоремы Геллмана - Фейнмана, что энергия VN равна сумме кулоновских взаимодействий пар ион - заряд, если только все расстояния таковы, что исключается перекрытие электронных облаков ионов. Если окажется, что это является чрезмерным упрощением для VN, значит должны быть существенны искажения ионных зарядов. [8]
Если атомы находятся на достаточно больших расстояниях Друг от друга, так, что электронные облака не перекрываются, То каждый электрон практически локализован у своего ядра. По мере сближения атомов возникает перекрытие электронных Облаков. Это означает, что в области перекрытия имеется некоторая вероятность нахождения обоих электронов. [9]
К полностью оборванных связей в боросиликатах может быть всего лишь около 10 - 20 % от общего числа связей. Выше было отмечено, что у близкодействующих ковалентных связей, снижающее энергию активации перекрытие потенциальных полей возможно при непосредственном перекрытии электронных облаков в условиях сближения локализованных связей. У стеклообразных систем этому способствует наличие мостиков из двухвалентных атомов VI группы элементов, придающих всему построению сетки связей подвижной шарнирный характер. Атомы кремния и кислорода связаны жесткими связями v с высокими силовыми постоянными. Локализованные связи на расстоянии относительно слабо взаимодействуют, и элементы структурного узла обладают несколькими степенями относительно свободного движения шарнирного характера. Имеют место формы движения: деформационные с изменением углов d между локализованными связями, вращательно-колебательные движения атомов кислорода по дуге г около оси Si. Si, нормальное к плоскости рисунка z - колебательное движение центрального атома кремния. [10]
Обнаружение в этих соединениях полупроводниковых свойств ( низкая концентрация носителей тока, высокая их подвижность и рост концентрации носителей тока с температурой и пр. Электронные мостики, обнаруженные им между ближайшими Л и 5 атомами в соединениях АШВУ, можно рассматривать как области перекрытия электронных облаков, аналогично германию и кремнию. Однако из-за разницы в химической природе атомов, образующих соединение, связь между ними не может быть чисто ковалентной. Поэтому электронные облака, связывающие атомы, должны быть асимметричны. [11]
Одной из характерных черт колебательных спектров комплексов являются особенности, связанные с наличием атома в центре комплекса, который по своей массе в большом числе изучаемых соединений резко превосходит атомы окружающих лигандов. Этот тяжелый атом нарушает кинематическую связь колебаний отдельных лигандов, расположенных вокруг центрального атома. При отсутствии заметного перекрытия электронных облаков лигандов это приводит к тому, что колебания каждого из лигандов совершаются почти независимо от наличия или отсутствия другого лиганда. [12]
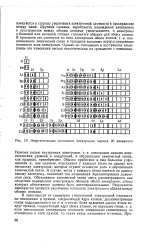 |
Энергетические состояния электронов первых 20 элементов. [13] |
Обычно прибегают к еще большим упрощениям и, как правило, отыскивают у каждого атома по одному или нескольку электронов, которые играют основную роль в образовании химической связи. В случае, когда у каждого атома имеется по одному такому электрону, возникает так называемая двухзлектронная химическая связь. Образование химической связи здесь рассматривается как следствие перекрытия электронных облаков обоих электронов, спины которых обязательно должны быть антипараллельными. Результатом перекрытия является увеличение плотности электронного облака между обоими атомами. [14]
О, характеризующий отклонение Н - связи от линейной. Свойства водородной связи, возникающей в результате перекрытия электронных облаков ОН-группы и электронодонорной молекулы, очевидно, должны зависеть от всех указанных геометрических параметров водородного мостика. [15]
Страницы: 1 2