Перенос - электрический ток
Cтраница 2
С дефектами А0 они могут объединяться в комплексы АОС, также, очевидно, не участвующие в переносе электрического тока. [16]
Если, однако, число этих электронов относительно мало, то наряду с ними существенную роль в переносе электрического тока могут играть вакантные места, или дырки, оставленные оторвавшимися электронами. При этом электронные дырки должны вести себя таким же образом, как электроны с положительным зарядом. [17]
Растворы и расплавы солей, растворы кислот и щелочей, называемые электролитами, относятся к проводникам второго рода, в которых перенос электрического тока осуществляется ионами. В проводниках первого рода, например металлах, ток переносится электронами. При прохождении электрического тока через электролит на электродах происходит разряд ионов и выделяются соответствующие вещества. Этот процесс называется электролизом. Аппарат, в котором осуществляется электролиз, называется электролизером или электролитической ванной. [18]
Электрон, участвующий в этом равновесии, хотя и не является свободным, однако он слабо связан и легко может участвовать в переносе электрического тока. [19]
 |
Электролиз с диафрагмой. [20] |
Анодное пространство отделяется от катодного пористой перегородкой, которая препятствует диффузии газов и растворов, но не мешает прохождению ионов, что обеспечивает перенос электрического тока. [21]
Следует подчеркнуть, что е -, фигурирующее в формулах (8.6) - (8.8), - не средняя тепловая энергия электронов, равная a / zkT, a средняя энергия электронов, участвующих в переносе электрического тока. [22]
АФПОЛН практически равен падению потенциала в толще оксидной пленки. Перенос электрического тока в твердых электролитах ( в частности, окислах металлов) определяется их полупроводниковой природой. [23]
При использовании катионитовой мембраны в катодную камеру из анодной могут переходить катионы железа, поэтому для исследований применялись анионитовые мембраны. Перенос электрического тока через анионитовую мембрану осуществляется сульфат-ионами, переходящими из католита в анолит. Увеличение концентрации сульфат-ионов в анолите благоприятствует процессу окисления ионов железа, так как для образования Fe2 ( S04) 3 необходим их избыток. [24]
 |
Прибор для измерения. [25] |
Перенос электрического тока осуществляется ионами, поэтому вполне естественно, что с уменьшением их числа в единице объема уменьшается и ток. Чтобы можно было сопоставлять электропроводности растворов различных электролитов, их значения необходимо выражать в единицах, не зависящих от концентрации. [26]
Как известно, при прохождении электрического тока через растворы электролитов на электродах происходит разряд ионов и протекают связанные с этим химические реакции. Протекание процесса электролиза определяется переносом электрического тока в жидкости и условиями разряда присутствующих в растворе ионов электролита. [27]
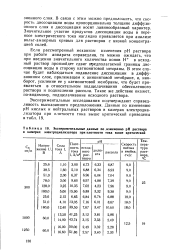 |
Экспериментальные данные по. изменению рН раствора в камерах электродиализатора при плотности тока выше критической. [28] |
В связи с этим можно предположить, что рость диссоциации воды пропорциональна толщине диффузионного слоя и диссоциация носит лавинообразный характер. Значительное участие продуктов диссоциации воды в переносе электрического тока наглядно проявляется при анализе вольт-амперных кривых для растворов с низкой концентрацией солей. [29]
Средняя энергия электронов, участвующих в переносе электрического тока, в различных проводниках различна, поэтому при переходе из одного проводника в другой электроны либо пополняют недостаток своей энергии, отнимая ее вблизи контакта у атомов проводника, в который они перешли, либо, наоборот, передают этим атомам избыток энергии. В первом сдучае теплота Пельтье поглощается, а во втором выделяется. [30]
Страницы: 1 2 3 4