Перенос - электричество
Cтраница 3
В переносе электричества, помимо ионов растворенных в воде солей участвуют, также Н и ОН -, образующиеся в результате диссоциации молекул самой воды. [31]
Вклад в перенос электричества в растворах полиэлектролитов вносят как противоионы, так и полиион. Интересной особенностью полиэлектролитов является то, что при условиях, когда их можно считать свободно проницаемыми для растворителя клубками, их электропроводность не зависит от молекулярной массы. [32]
В растворе перенос электричества осуществляется ионам и причем каждый вид ионов переносит определенное количество электричества в зависимости от содержания данных ионов в растворе, их валентности и скорости движения в электрическом поле. [33]
Детали процессов переноса электричества в органических полупроводниках выяснены недостаточно. В большой мере это обусловлено малочисленностью надежных экспериментальных данных для хорошо охарактеризованных материалов. Обычные для полупроводников измерения в этом материале хотя и полезны, но не настолько удовлетворительны, как в неорганических полупроводниках, прежде всего из-за малой константы Холла и неопределенности процессов переноса. [34]
Действительно, одинакового переноса электричества можно достигнуть либо за счет быстрого движения малого числа ионов, либо за счет медленного движения соответственно большего числа ионов. Чем больше скорость движения данных ионов в нормальных условиях, тем большую концентрацию их нужно взять, чтобы уравнять скорость движения этих ионов со скоростью движения каких-либо других ионов. Наконец, последнее условие заключается в тщательном определении перепада потенциала, заставляющего перемещаться границу соприкосновения растворов. Этого возможно достигнуть либо специальными приспособлениями, либо тщательным учетом сопротивления в различных частях прибора. [35]
Если в переносе электричества участвуют и дырки и электроны, то картина эффекта Холла значительно усложняется. [36]
Если в переносе электричества участвуют и дырки, и электроны, то картина эффекта Холла значительно усложняется. В выражение для магнитной силы входит произведение скорости частицы на заряд; поскольку для электронов и дырок, участвующих в переносе тока, и знак ( направление) скорости, и знак заряда противоположны, то направления сил, действующих на них, одни и те же, и отклоняться они будут в одну и ту же сторону. [37]
Хотя в переносе электричества через растворы электролитов участвуют все ионы, все же вследствие различия их скоростей, концентраций и зарядов доля их участия в переносе неодинакова. [38]
В толще раствора перенос электричества осуществляется двумя переносчиками одновременно. Положительные ионы движутся в одну сторону, а отрицательные - в другую. Но через границу раздела электрод - раствор электричество переносится только одним видом ионов. Представим себе, например, электролизер, в который налит раствор AgNOa и помещены два серебряных электрода. [39]
 |
Удельное сопротивление различных проводников при 18 С ( ом-см. [40] |
В растворах электролитов перенос электричества осуществляется за счет перемещения ионов. Анионы в электрическом поле движутся к положительно заряженному электроду-аноду, катионы-к отрицательному электроду-катоду. Скорость движения ионов в растворах по сравнению со скоростями движения электронов в металлах мала, поэтому электропроводность, например, меди и серебра примерно в 1 000 000 раз больше электропроводности растворов. [41]
В растворах электролитов перенос электричества осуществляется за счет перемещения ионов. Анионы в электрическом поле движутся к положительно заряженному электроду - аноду, катионы - к отрицательному электроду - катоду. Скорость движения ионов в растворах по сравнению со скоростями движения электронов в металлах мала, поэтому электрическая проводимость, например, меди и серебра примерно в 1 000 000 раз больше проводимости растворов. [42]
Согласно обеим схемам перенос электричества осуществляется за счет перескока протона от одной частицы к другой. [43]
В растворах электролитов перенос электричества осуществляется ионами, и, следовательно, электропроводность таких растворов будет зависеть от концентрации ионов и скорости их движения. [44]
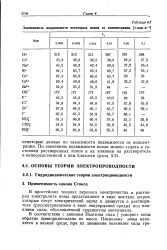 |
Зависимость подвижности некоторых ионов от концентрации [ г-экв - л - 1 ]. [45] |
Страницы: 1 2 3 4