Перенос - группа
Cтраница 3
Леигмюр показал, что правило Дюкло - Траубе может быть использовано для расчета энергии переноса группы - СН2 - из объема раствора в газовую фазу. [31]
Имеется ряд данных, указывающих на участие фолиевой кислоты как в синтезе, так ив переносе фсущшщных групп ( и вообще одноуглеродистых фрагментов) при образовании ряда веществ в организме. [32]
 |
Механизм действия трансфераз при двойной перестановке участников реакции. Объяснения в тексте. [33] |
В тканях животного организма, а также у микроорганизмов и высших растений найдены все три типа реакций переноса гликозиль-ных групп, являющихся разными путями биосинтеза олиго - и полисахаридов; остается неразрешенным вопрос о том, какая из групп ферментов имеет наибольшее значение в данном организме или ткани. Тем не менее имеющиеся данные представляют интерес. [34]
Как уже отмечалось, при инкубации уропор-фириноген - Ш - консинтетазы с ПБГ пиррол не изменяется ( скажем, путем переноса амино-метильной группы в другое а-положение) и не используется для образования порфириногена. С другой стороны, в то время как скорость утилизации ПБГ в системе, содержащей ПБГ, уропорфириноген-1 - синтетазу и уропорфи-риноген - Ш - косинтетазу, определяется прежде всего концентрацией уропорфириноген-1 - синтетазы, реакция идет менее быстро, если уропорфириноген - Ш - косинтетаза исключается из состава реакционной смеси. [35]
Рассмотренный механизм обмена серы в политионатах полностью согласуется с механизмом разных реакций их образования и разложения, которые также совершаются путем переноса целых сульфитных и тиосульфатных групп, как показали при помощи радиоактивной серы Р. К. Еременко и автор ( стр. [36]
Естественно, что часть мета-производных, являющихся продуктами аномального замещения, образуется из 1 2 4-триалкилбензола путем деалкплирования алкильной группы от первого углеродного атома или переноса 1-алкилыюй группы в другое ядро. [37]
 |
Алкнлирование изопентенилпирофосфатом в биосинтезе ауроглау.| Ацилирование бензола. [38] |
Электрофилы, ответственные за алкилирование ароматических соединений в живых системах, генерируются из таких соединений, как аминокислота метионин ( перенос метильных групп) и изопентенилпирофосфат ( перенос групп GS, как в биосинтезе плесневого продукта ауроглауцина, рис. 5.20; см. гл. [39]
Ферментативными реакциями являются реакции гидролиза, гидрирования и дегидрирования ( присоединение водорода к молекулам субстрата или отщепление водорода от его молекул), реакции окисления ( перенос электронов), реакции переноса групп фосфорной кислоты и органических групп. Исследованием ферментативных реакций занимается биохимия. [40]
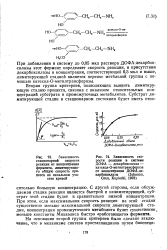
При добавлении в систему до 0 05 мкл раствора ДОФА-декарбок-силазы этот фермент определяет скорость реакции, в присутствии декарбоксилазы в концентрации, соответствующей 0 5 мкл и выше, лимитирующей стадией является перенос метйльной группы с помощью катехол - О-метилтрансферазы. [42]
 |
Некоторые ферментативные реакции переноса фосфорила и нуклеотидила, включающие нуклеозидполифосфатные эфиры 40а. [43] |
Оба фермента нуждаются в ионах магния, как в кофакторе, и если р-фосфорильная группа АТР координирована с ионом магния, как продемонстрировано методом 31Р - ЯМР, тогда нуклеофильная атака будет приводить к переносу пирофос-форильной группы. Однако необходимы дальнейшие исследования для того, чтобы выяснить истинный механизм действия этих ферментов. [44]
Рассмотрите кинетическое поведение системы для следующего простейшего случая ошибочной ориентации субстрата в активном центре фермента: фермент Е катализирует односубстратную реакцию, в которой нормальный субстрат PQ связывается на ферменте в центре Р, что позволяет осуществить перенос группы Q к центру Q фермента. Самопроизвольное отщепление Q от Q регенерирует свободный фермент. Поскольку Р имеет сродство лишь с Р, ошибочная ориентация исключается. Если же субстрат имеет строение. Хотя группировка R имеет то же сродство к Р, как и Р, она способна связываться отчасти и с Q, в результате чего RQ иногда образует с ферментом комплекс с обратной ориентацией, не способный к расщеплению. В обоих случаях субстрат связывается с ферментом обратимо, причем в каждый момент времени одна молекула фермента может связывать лишь одну молекулу субстрата. [45]
Страницы: 1 2 3 4