Гомогенный перенос - электрон
Cтраница 1
Гомогенный перенос электронов в растворе может осуществляться и за счет продуктов реакции. [1]
Процесс, включающий гомогенный перенос электрона между вторым катион-радикалом и интермедиа-том ( полученным в реакции нуклеофила с первым катион-радикалом), при котором количество регенерируемого субстрата равно половине концентрации электрохимически генерированного катион-радикала субстрата. Иногда символом Е обозначают как химическую, так и электрохимическую стадии переноса электрона. [2]
Иначе обстоит дело с гомогенным переносом электрона, который в тех случаях, когда он достаточно экзотермичен, может приводить к углеводородам, находящимся в возбужденном состоянии Для простоты можно считать, что удаление электрона происходит с высшей связывающей молекулярной орбитали с образованием первого возбужденного синглета или триплета. [3]
На основании данных, полученных с помощью метода ЛВА [125], предположили, что скоростьопредсляющей стадией этого процесса является гомогенный перенос электрона. [4]
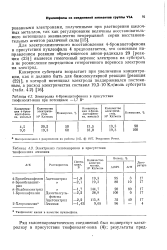 |
Электролиз 4-бромацетофенона в присутствии тиофенолят-иона при потенциале - 1 7 Ва.| Электролиз галогенаренов в присутствии тиофенолята аммония. [5] |
Для электрохимического восстановления 4-бромацетофенона в присутствии нуклеофила 4 предполагается, что основным направлением реакции образующегося анион-радикала 23 [ реакция ( 23) ] является гомогенный перенос электрона на субстрат, а не реокисление посредством гетерогенного переноса электрона на электрод. [6]
Фенил-1 3-дитиолан дает лишь 5 % бензальдегида. Снятие 1 3-ди-тиановой защиты гомогенным переносом электрона с катион-радикала ТТА обсуждается в гл. [7]
По длине волны наблюдаемое излучение обычно соответствует полосе в спектре флуоресценции данного углеводорода, обусловленной переходом из первого возбужденного состояния в основное состояние. Энергия, выделяющаяся при гомогенном переносе электрона, определяется разностью окислительно-восстановительных потенциалов донора и акцептора плюс небольшой энтропийный член [ 911; во многих случаях, когда наблюдается электрохеми люминесценция, этой энергии недостаточно для непосредственного образования синглетного состояния. [8]
Таким образом, последние стадии электрохимического процесса включают химические реакции, протекающие как до, так и после переноса электрона. Наконец, некоторые из образовавшихся частиц легко окисляются как иа электроде, так и путем гомогенного переноса электрона в растворе. [9]
В этом разделе рассматриваются такие реакции нуклеофильного галогенирования. Как обсуждалось в разд. Первый процесс гомогенного переноса электрона может в некоторых случаях быть причиной снижения выхода по току. Окисление ароматических соединений в присутствии иодид-ионов обычно не приводит к иодароматическим соединениям, так как при действии иодид-иона происходит исключительно восстановление катион-радикалов. [10]
Майрановский считает, что рассмотренные ранее реакции супероксидного иона, образующегося после переноса электрона при одноэлектронном восстановлении, нельзя, по-видимому, относить к этому обсуждаемому типу превращений, поскольку ион OJ взаимодействует с субстратами необратимо, не возвращаясь в реакцию, и есть основания считать, что этот ион действует как ну-клеофильный реагент, а не как донор электронов. Это может быть связано с очень большим различием в энергиях высшей занятой молекулярной орбитали OJ - и низшей вакантной молекулярной орбитали субстрата, приводящим к высокой энергии активации и низкой скорости переноса электрона. Электродные реакции с органическими переносчиками электронов, протекающие по такому механизму, весьма перспективны для изучения кинетики гомогенного переноса электрона и должны дополнить существующие методы изучения констант скорости этого переноса, а также моделировать переход от гетерогенных условий к гомогенным, что в препаративном электросинтезе может способствовать снижению потенциала рабочего электрода, устранить ингибирующее влияние электрода на перенос электрона и в целом повысить экономичность процессов. [11]
В литературе имеется немного сообщений о реакциях с переносом электрона с участием карб-оксилатов. Шмидт и Стехан i [94] обнаружили, что электрохимически генерированный катион-радикал ТБФА способен восстанавливать различные алифатические карбоксилаты. Качественно это было продемонстрировано с помощью циклической вольтамперометрии ТБФА без добавок и в присутствии пелар-гоната тетрабутиламмония в различных концентрациях. Ток анодного пика при генерировании катион-радикала ТБФА возрастает на величину каталитического тока, которая зависит от концентрации карбоксилата. Спектроэлектрохимическое исследование этого гомогенного переноса электрона позволяет перейти к количественному описанию. Так, спектроскопически исследовалось расходование катион-радикала ТБФА; реакция имеет первый порядок как по катион-радикалу, так и по карб-оксилату и обратный первый порядок по ТБФА. [12]
Здесь имеет смысл кратко остановиться на вопросе о применимости конкурентных методов для изучения химических реакций с участием катион-радикальных интермедиатов. Эти реакции протекают через быстрое обратимое взаимодействие окислителя с ароматическим соединением, приводящее к образованию соответствующего катион-радикала. Лимитирующей стадией является идущая после равновесия химическая реакция, такая, как отщепление протона. Соотношение двух ион-радикалов, определенное по значению / СРавн гомогенных реакций переноса электрона, оказывает влияние на полученную таким образом относительную реакционную способность. Поэтому при простом применении этого метода следует соблюдать осторожность, особенно если заранее известно, что скорость гомогенного переноса электрона велика и равновесие сильно смещено в одну сторону. [13]
Страницы: 1