Боразола
Cтраница 2
Боразол B3N3H6 по своим свойствам во многом аналогичен бензолу, поскольку изоэлектронен с ним и имеет приблизительно такой же молекулярный вес. [16]
Боразол может быть получен двумя способами: а) нагреванием диборана и аммиака до250 С, б) нагреванием литийборгидрида и хлорида аммония до 300 С. [17]
Боразол и его производные представляют как теоретический, так и практический интерес. Имеются, например, маслостойкие и термостойкие бороорганические соединения. Производные боразола могут применяться также в качестве ракетного топлива. [18]
Боразол может быть получен двумя способами: 1) нагреванием диборана и аммиака до 250 С, 2) нагреванием литийборгидрида и хлорида аммония до 300 С. [19]
 |
Степень ионности связи С - Me по Полингу. [20] |
Боразол, как и карбораны, также проявляет сходство с бензолом, хотя в силу полярности связей N-В можно ожидать, что он более реакционноспособен. [21]
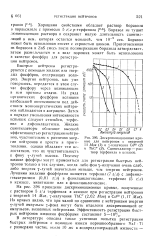 |
Дискриминационные кривые для нейтронов с энергией 14 Мэв ( / и у-излучения Со60 ( 2 и ThC (. 3. Сцинтнллятор - раствор терфенила в ксилоле. [22] |
Боразол не тушит люминесценции раствора и сохраняет малую длительность сцинтилляций в нем, которая остается меньшей, чем 10 сек. Боразол может быть использован вместе с сернистым цинком. Приготовленная из боразола и ZnS смесь после полимеризации боразола затвердевает, затем размельчается и в виде порошка может быть использована в качестве фосфора для регистрации нейтронов. [23]
Боразол неустойчив к щелочам. Они его разлагают с образованием аммиака, борной кислоты и водорода. [24]
Боразол, как и бензол, представляет собой жидкость, которая значительно более химически устойчива, чем гидриды бора и их производные. Однако по сравнению с бензолом более реакционноспособен: медленно окисляется на воздухе, склонен к реакциям замещения и присоединения. [25]
Боразол был открыт в 1926 г. Штоком и Поландом [ 171, С химической точки зрения боразол представляет циклический амидборгидрид. На основании химических и физических свойств и изучения диффракции электронов ему придается [67, 68] циклическая формула с тремя атомами бора и тремя атомами азота в цикле, причем длина связи В-N равна 1 44 А. [26]
Боразол и его производные представляют как теоретический, так и практический интерес. Имеются, например, маслостойкие и термостойкие бороорганические соединения. Производные боразола могут применяться также в качестве ракетного топлива. [27]
Свойства боразола очень похожи на свойства бензола. Он кипит при 55 С, горит, является хорошим растворителем. [28]
Пиролиз боразола начинается при температуре - 300 С. [29]
Производные боразола, полученные при замещении атомов водорода при азоте ( но не при боре), по химическим свойствам сходны с боразолом. [30]
Страницы: 1 2 3 4