Борат-ионы
Cтраница 1
Борат-ионы - по образованию окрашенного пламени при сгорании борнометилового или борноэтилового эфиров. [1]
Борат-ионы или борная кислота образуют с этанолом C2HsOH в присутствии серной кислоты сложный этиловый эфир борной кислоты ( С2Н50) 3В, который окрашивает пламя в зеленый цвет. [2]
Борат-ионы можно обнаружить в анализируемой смеси твердых веществ. Для этого в фарфоровую чашку или тигель помещают небольшое количество твердой смеси, прибавляют 3 - 5 капель воды, около 0 5 мл концентрированной серной кислоты и 0 5 - 1 мл этилового спирта. Смесь хорошо перемешивают и поджигают. [3]
Борат-ионы, открытие 176, 200 Бром-ион, открытие 159, 196 Бромат-ион, открытие 185, 201 Бромкрезолпурпурный 34 Бромтимолсиний 35 Бромфенолсиний 35 Бумага фильтровальная 20 ел. [4]
Борат-ионы ВО, В4О, открывают с помощью куркумовой бумаги - бумаги, обработанной раствором органического красителя - кур-кумина. Соли борной кислоты окрашивают в кислой среде куркумовую бумагу в розовый цвет. Щелочи и аммиак изменяют окраску на синюю или буровато-зеленую. [5]
Как открывают борат-ионы в систематическом ходе анализа. [6]
Как уже упоминалось, борат-ионы практически не поглощаются сильнокислотными катионообменниками ( Dv 1) из солянокислых растворов. При концентрации НС1 выше 4 М ионы 1п3 поглощаются в незначительной степени. Сорбция ионов Т13 из разбавленных растворов НС1 очень низка. [7]
Какими реакциями обнаруживают силикат - и борат-ионы. [8]
Бура, диссоциирующая в водном растворе на натрий - и борат-ионы, не высаживает поливиниловый спирт при любой концентрации. Осаждающая способность электролитов зависит от теплот их гидратации. На рис. 15.1 приведена зависимость пороговой концентрации при осаждении калиевыми, натриевыми и аммонийными солями от теплот гидратации анионов. [9]
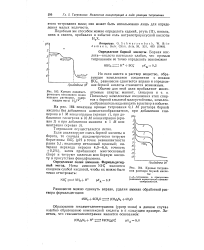 |
Кривая ацидимет-рического титрования ионов кальция раствором, содержащим ионы H2Y2 -.| Кривые титрования раствора борной кислоты. [10] |
Если анализируют смесь борной кислоты и бората, то сначала ацидиметрически титруют борат-ионы ВО2 ( рН в точке эквивалентности равен 5 1; индикатор метиловый красный; интервал перехода окраски 4 0 - 6 6; точность 0 2 %), затем прибавляют многоосновный спирт и титруют щелочью всю борную кислоту в присутствии фенолфталеина. [11]
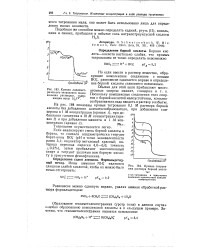 |
Кривая ацидимет-рического титрования ионов кальция раствором, содержащим ионы H2Ya -.| Кривые титрования раствора борной кислоты. [12] |
Если анализируют смесь борной кислоты и бората, то сначала ацидиметрически титруют борат-ионы ВОа ( рН в точке эквивалентности равен 5 1; индикатор метиловый красный; интервал перехода окраски 4 0 - 6 6; точность 0 2 %), затем прибавляют многоосновный спирт и титруют щелочью всю борную кислоту в присутствии фенолфталеина. [13]
Электрофореграммы обычно проявляют теми же реагентами, что и бумажные хроматограммы, если развитию окраски не препятствуют присутствующие в буфере ионы, например борат-ионы. [14]
Борную кислоту или борат-ионы можно определять после проведения соответствующих реакций с HF, в результате которых образуются тетрафторбо - - рат-ионы. [15]
Страницы: 1 2