Переход - электрон
Cтраница 2
Переход электрона из овалентной связи к атому индия требует значительно меньше энергии, чем через запрещенную зону AW, поэтому введение атома индия в решетку кремния приводит к появлению уровня акцептора Wa вблизи от потолка валентной зоны, который при очень низких температурах остается свободным. При небольшом повышении температуры один из валентных электронов покидает валентную зону и занимает уровень примеси ( рис. 21, б), оставляя после себя в валентной зоне свободный уровень - дырку. Энергия AWaWa-Ws, которую необходимо сообщить валентному электрону для перевода его на примесный уровень, называют также энергией активизации примеси. Электроны валентной зоны переходят на уровень примеси даже при низких температурах, образуя в валентной зоне большое количество дырок. [16]
Переход электрона из одной зоны в другую осуществляется путем поглощения или отдачи им энергии, достаточной для переброса электрона через запрещенную зону. [17]
 |
Атомы гелия ( а и кислорода ( б. [18] |
Переход электрона с одной орбиты на другую связан с изменением его энергетического уровня. [19]
Переход электрона из полупроводника в диэлектрик определяется свойствами границы раздела кремний - двуокись кремния, которые в свою очередь зависят от объемных свойств полупроводника. Энергетические уровни ловушек, находящихся на поверхности материала, располагаются в запрещенной зоне. Такие поверхностные состояния можно разделить на два типа: состояния, расположенные на границе раздела диэлектрик - полупроводник, и состояния, расположенные в слое двуокиси кремния. Каждый тип состояний обусловлен соответствующим видом взаимодействия. [20]
Переход электрона на более низкий уровень сопровождается выделением избытка энергии в виде излучений. В веществах, образованных совокупностью атомов, вследствие влияния соседних атомов энергетические уровни несколько изменяются, образуя энергетические зоны. Эти зоны отделяются областями, в которых электроны не могут находиться, поэтому они называются запрещенными зонами. Если у атома не хватает электронов для заполнения всех уровней, то внешние орбиты могут оказаться частично или полностью не занятыми. Следовательно, и энергетические зоны, соответствующие разрешенным уровням, могут быть заполненными или свободными. [21]
Переход электрона на более низкий энергетический уровень с излучением кванта света может произойти с помощью электромагнитного воздействия. Такую рекомбинацию ( такой переход) называют вынужденной, индуцированной или стимулированной. Следовательно, квант света с определенной частотой может не только поглощаться полупроводником, но и вызывать добавочное индуцированное излучение. [22]
Переход электрона на глубокий примесный центр и с этого центра в валентную зону также может сопровождаться излучением кванта соответствующей энергии. Однако вероятность таких излучательных переходов в Ge и Si тоже невелика. [23]
Переход электронов с несвязывающих n - орбиталей на связывающую о-орби-таль сопровождается выигрышем энергии, вследствие чего уровень энергии связывающих о-орбиталей значительно ниже уровня энергии п-орбиталей. [24]
Переход электронов с несвязывающих n - орбиталей на связывающую я-орби-таль сопровождается выигрышем энергии, меньшим, однако, чем при образовании - а-связи. Поэтому уровень энергии связывающих я-орбиталей располагается между уровнями энергии / г-орбиталей и связывающих а-орбиталей. [25]
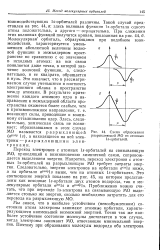 |
Схема образования разрыхляющей МО из ls - орбиталей. [26] |
Переход электронов с атомных ls - орбиталей на связывающую МО, приводящий к возникновению химической связи, сопровождается выделением энергии. Напротив, переход электронов с атомных ls - орбиталей на разрыхляющую МО требует затраты энергии. [27]
 |
Энергетическая схема образования МО при взаимодействии U-орбиталей двух одинаковых атомов.| Энергетическая схема образования молекулы водорода. [28] |
Переход электронов с атомных ls - орбиталей на связывающую МО, приводящий к возникновению химической связи, сопровож - дается выделением энергии. Напротив, переход электронов с атомных ls - орбиталей на разрыхляющую МО требует затраты энергии. [29]
 |
Энергетическая схема образования молекулы водорода. [30] |
Страницы: 1 2 3 4