Борогидрид - калий
Cтраница 1
Борогидрид калия плохо растворим в триглимс и в тетрагвдро-фуране, но сто можно использовать в виде суспензии в этих растворителях. [1]
Борогидрид калия плохо растворим в триглиме и в тетрагидро-фуране, но его можно использовать в виде суспензии в этих растворителях. [2]
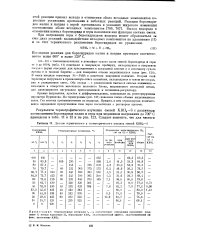 |
Данные термического и гапометрического анализа смесей КВШ-S. [3] |
Последняя реакция для борогидридов калия и натрия протекает соответственно выше 600 и выше 520 С. [4]
Месмер и Джолли [17] нашли, что твердый борогидрид калия, взаимодействуя с молекулярным дейтерием при 50 атм, за 72 часа обменивает свой водород на дейтерий на 84 % от равновесной концентрации. [5]
Хлористый цинк хорошо растворим в эфире, но борогидрид калия совсем норастворим в нем, тем не менее перемешиванием суспензии борогидрида в эфирном растворе хлористого цинка в течение 5 - 30 час. [6]
Ссылки, приведенные для борогидрида лития, борогидрида натрия и борогидрида калия, не являются исчерпывающими. [7]
Метод основан на том, что сахароза не реагирует с борогидридом калия, так как не имеет в молекуле карбонильной группы. Таким образом, оптическое вращение сахарозы не изменяется при обработке борогидридом калия. Глюкоза при восстановлении боргидридом калия образует сорбит, оптическое вращение которого практически равно нулю. [8]
Исследуемый полисахарид сначала окисляют периодатом до полиальдегида и полиальдегид восстанавливают борогидридом калия до полиола. Затем полиолы подвергают ацетолизу и образующиеся ацетаты спирта разделяют методом ГЖХ. Глюкозный остаток, соединенный связями 1 - 4, образует эритриттетраацетат, а невосстанавливающиеся концевые группы дают начало глицеринтриацетату. Поэтому относительное содержание этих соединений, определенное методом ГЖХ, может служить мерой степени полимеризации линейного полисахарида. [9]
Построение кривых выхода водорода очень четко выявляет два основных направления реагирования борогидрида калия с серой в процессе нагревания: реакцию образования боросульфида калия по уравнению ( II), протекающую при 232 - 300 С, и для смесей с избытком борогидрида калия - термическое разложение КВН4 по уравнению ( III) при более высоких температурах. [10]
Селективное восстановление кетогругаш в кетокисдоц ( И-4); карбоксильная группа борогидридом калия ( натрия) не восстав ливается. [11]
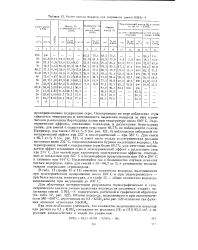 |
Расчет выхода водорода при нагревании смесей КВШ-S. [12] |
Одновременно по мере добавления серы снижается температура и интенсивность выделения водорода за счет термического разложения борогидрида калия при температуре около 600 С. Эндотермические эффекты, отвечающие плавлению и разложению борогидрида калия, для смесей с содержанием серы выше 66 7 % не наблюдаются совсем. [13]
Объяснить отклонение количества выделяемого водорода при термическом разложении от теоретического, за счет распыления и уноса частиц борогидрида калия, по-видимому, нельзя, так как вероятность потери борогидрида наибольшая при стехиометрическом отношении, где реакция проходит особенно бурно, а именно для этого состава мы имеем максимальный выход водорода. [14]
В качестве восстановителей для нанесения химического Ni-В - покрытия предлагается использовать следующие соединения бора: борогидриды - борогидрид натрия NaBH4, борогидрид калия КВН4, цианоборогидрид натрия NaBHsCN, триметоксиборогидрид натрия МаВН ( ОСН3) з, борогидрид тетраметиламмония ( CH3) 4 - NB4; бор-азотные соединения - боразаны R3N - BH3, боразены R2N - BH2, боразолы ( RNBH) 3, где R - водород, алкил, арил или амин. [15]
Страницы: 1 2 3