Длинный период - периодическая система
Cтраница 1
Длинные периоды периодической системы можно описать как короткие, в которые включено десять дополнительных элементов. Первые три элемента длинного периода между аргоном и криптоном - металлы калий, кальций и скандий - по свойствам напоминают соответствующие металлы предшествующего короткого периода - натрий, магний и алюминий. Остальные элементы длинного периода - титан, ванадий, хром, марганец, железо, кобальт, никель, медь, цинк и галлий - не имеют родственных им более легких аналогов; они по своим свойствам не очень похожи ни на один легкий элемент. [1]
Ионы элементов малых периодов и концов длинных периодов периодической системы имеют тенденцию сохранять неизменную валентность и принимать структуру заполненных оболочек. Переходные элементы имеют переменную валентность, образуют стабильные ионы с незаполненными d - оболочками и могут давать окрашенные магнитные, полупроводниковые соединения, катионы которых имеют электроны с непарными спинами. Можно сказать, что ионы с полузаполненными и заполненными подоболочками ( d5, Mn2; d10, Zn2) по своим свойствам находятся между двумя этими крайностями. [2]
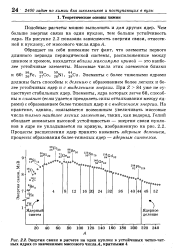 |
Энергия связи в расчете на один нуклон в устойчивых четно-четных ядрах со значениями массового числа А, кратными 4. [3] |
Обращает на себя внимание тот факт, что элементы первого длинного периода периодической системы, расположенные между цинком и хромом, находятся вблизи максимума кривой - это наиболее устойчивые элементы. [4]
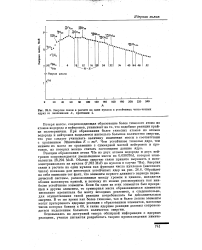 |
Энергия связи в расчете на один нуклон в устойчивых четно-четных ядрах со значениями А, кратными 4. [5] |
Энергия связи в расчете на один нуклон как функция числа нуклонов ( массового числа) показана для некоторых устойчивых ядер на рис. 26.6. Обращает на себя внимание тот факт, что элементы первого длинного периода периодической системы, расположенные между хромом и цинком, находятся вблизи максимума кривой, и поэтому их можно рассматривать как наиболее устойчивые элементы. Если бы один из этих элементов был превращен в другие элементы, то суммарная масса образовавшихся элементов несколько превышала бы массу исходных реагентов, а следовательно, для осуществления такой реакции потребовалась бы дополнительная энергия. В то же время как более тяжелые, так и более легкие элементы могут претерпевать ядерные реакции с образованием элементов, массовые числа которых близки к 60, и такие ядерные реакции должны сопровождаться выделением большого количества энергии. [6]
Анализ огромного материала по каталитическим свойствам веществ, собранного в трех томах справочника Каталитические свойства веществ, показал, что каталитические свойства в отношении реакции гидрогенизации проявляются главным образом у элементов ( и их соединений) длинных периодов периодической системы Д. И. Менделеева, преимущественно у металлов VI, VII, VIII и 16 групп. [7]
В качестве комплексообразователей при производстве красителей применяют металлы, ионы которых имеют незаполненные электронные орбитали и являются хорошими акцепторами электронов. Такими ком-плексообразователями являются катионы переходных элементов первого длинного периода Периодической системы Д. И. Менделеева: хром, кобальт, никель, медь, которые обладают незаполненными 3d -, 4s - и 4р - орбиталями. Эти орбитали способны заполняться неподеленными парами электронов лигандов. Лиганды предоставляют электронные пары для образования координационных связей с металлом. Помимо хрома, кобальта, никеля и меди способностью к образованию комплексных солей обладают цинк, марганец, железо, алюминий и другие металлы, но они не применяются для получения металлсодержащих красителей, так как образуют малостабильные или плохо растворимые в воде комплексы. Выбор металла для комплексообразования зависит от свойств того или иного класса красителей. [8]
Четвертый период является первым из так называемых длинных периодов периодической системы. Он начинается с появлением у атомов калия и кальция соответственно одного и двух 45-электронов, принадлежащих jV - оболочке. Заполнение ЗсС - состояний Ж - оболочки начинается у скандия и продолжается далее у так называемых переходных элементов. [9]
Четвертый период является первым из так называемых длинных периодов периодической системы. Он начинается с появлением у атомов калия и кальция соответственно одного и двух 45-электронов, принадлежащих jV - оболочке. Заполнение Зй-состояний УИ-оболочки начинается у скандия и продолжается далее у так называемых переходных элементов. [10]
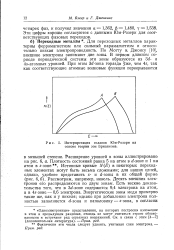 |
Интерпретация сплавов Юм-Розери на основе теории зон Бриллюэна. [11] |
Для переходных металлов характерны ферромагнетизм или сильный парамагнетизм и относительно низкая электропроводность. Джонсу [10], внешние электроны занимают две зоны. В первом длинном периоде периодической системы эти зоны образуются из 3d - и 45-атомных уровней. [12]
Как известно, к переходным металлам относятся элементы дополнительных подгрупп периодической системы. Эти элементы обладают свойствами, характерными для металлов. Они занимают средние части длинных периодов периодической системы от Se до Ni, от Y до Pd, от La до Pt. К ним же относятся все актиноиды. Для этих элементов характерна незавершенность d - оболочки и наличие нескольких валентных состояний. [13]
Как известно, к переходным металлам относятся элементы дополнительных подгрупп периодической системы. Эти элементы обладают свойствами, характерными для металлов. Они занимают средние части длинных периодов периодической системы от Se до Ni, от Y до Pd, от La до Ft. К ним же относятся все актиноиды. В свободных атомах этих элементов происходит заполнение ( п - 1) с. Для этих элементов характерна незавершенность d - оболочки и наличие нескольких валентных состояний. [14]
Страницы: 1