Периодичность - свойство
Cтраница 2
О функции, которая соответствует периодичности свойств химических элементов. [16]
Необходимо в заключение отметить, что периодичность свойств А. Теряя один электрон, атомы элементов данной группы становятся подобными по своим свойствам атомам элементов предыдущей группы ( напр. Она сохраняется и при потере k электронов. Схожими свойствами обладают нейтральный А. [17]
По сравнению с малыми периодами, периодичность свойств в больших периодах носит более сложный, можно сказать, двоякий характер. [18]
Необходимо в заключение отметить, что периодичность свойств А. Теряя один электрон, атомы элементов данной группы становятся подобными но своим свойствам атомам элементов предыдущей грушш ( напр. Она сохраняется и при потере k электронов. Схожими свойствами обладают нейтральный А. [19]
Основу закона Д. И. Менделеева составляет открытая им периодичность свойств химических элементов. Она была убедительно доказана уже при самом возникновении закона, и все последующее развитие химической науки явилось развитием и подтверждением его идеи. [20]
Тем не менее Менделеев считал, что периодичность свойств здесь выступает достаточно ясно. [21]
Имеющие мировое значение работы Д. И. Менделеева наглядно выявили периодичность свойств химических элементов, которую можно было объяснить повторяемостью комбинаций в расположении электрических зарядов внутри атомов. [22]
По сути дела заново написана четвертая глава о периодичности свойств, существенно изменена седьмая глава, посвященная стереохимии неорганических соединений, и значительно расширено изложение учения о координационных соединениях. [23]
Влияние растворяющегося вещества, а также растворителя на периодичность свойств растворов можно наглядно проследить на примере растворов йода и некоторых других галогенов, а также интергалидов в органических растворителях. Как известно, йод в разных растворителях по-разному окрашивает раствор. Это связано с прочностью молекулярного соединения, образованного молекулами йода и молекулами растворителя. [24]
Однако возможность определения атомных весов на основе закона периодичности свойств химических элементов не является главным в открытии Д. И. Менделеева, в применении его закона к атомно-молекулярной теории. [25]
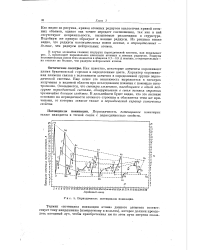 |
Периодичность потенциалов ионизации. [26] |
Периодичность потенциалов также находится в тесной связи с периодичностью свойств. [27]
Научной основой курса химии средней школы является учение о периодичности свойств и строении атомов элементов. На первоначальном этапе обучения в средней школе и ПТУ / техникумах и на подготовительных курсах много внимания уделяется атомно-молекулярной теории и основным законам химии. Поэтому указанный материал намеренно не рассматривается в пособии отдельно. [28]
Научной основой курса химии средней школы является учение о периодичности свойств и строении атомов элементов. На первоначальном этапе обучения в средней школе и ПТУ, техникумах и на подготовительных курсах много внимания уделяется атомно-молекулярной теории и основным законам химии. Поэтому указанный материал намеренно не рассматривается в пособии отдельно. [29]
Периодичность потенциалов ионизации также находится в тесной связи с периодичностью свойств. [30]
Страницы: 1 2 3 4