Пероксигруппа
Cтраница 1
Пероксигруппа - кислородная цепочка - О-О -, ( кислородный мостик), в которой атомы кислорода связаны между собой с-связью. [1]
Пероксигруппу можно ввести в некоторые органические молекулы при обработке их гидропероксидом в присутствии хлорида меди ( 1) или других катализаторов, например солей кобальта и марганца [198]; выходы обычно очень высокие. Как и в реакциях с N-бромосукцинимидом ( см., например, реакцию 14 - 2), замещению подвергается главным образом бензильный, аллильный и третичный водород. Реакция идет по механизму свободнорадикального типа с участием радикала ROO, образующегося из ROOH под действием иона металла. [2]
Однако обмена алкоксигруппы на пероксигруппу в случае ароматических германийорганических соединений, например трифенилгермания, не происходит. [3]
Реакция триалкплборных соединений с кислородом легко протекает с образованием лишь двух пероксигрупп. [4]
Характерно, что температурный коэффициент изменения скорости процесса разложения формирующихся в ПВХ пероксигрупп ( 19 7 ккал / моль) аномально низок 283 по сравнению с этим коэффициентом процесса разложения перекисных групп других озонированных полимеров, для которых энергия активации равна 30 - 35 ккал / моль. Низкую величину Егкг перекисных группировок в озонированном ПВХ следует связывать с каталитическим действием HG1, элиминирующего из полимера в ходе реакционного процесса. При этом возможно как гемолитическое, так и гетеролити-ческое ( под влиянием НС1) разложение пероксигрупп. [5]
Такое различие, несомненно, объясняется присутствием а-водорода при атоме углерода, содержащем пероксигруппу. [6]
Здесь будут рассмотрены четыре основных типа гемолитических реакций: отрыв водорода под действием свободных радикалов, радикальное замещение пероксигруппы, термическое разложение и реакции с ионами металлов. [7]
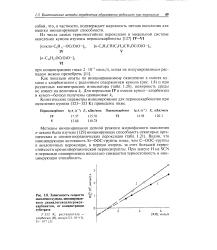 |
Зависимость скорости окисления кумола, инициированного дициклогексилперокси-карбонатом, от концентрации субстрата. [8] |
Видно, что инициирующая активность Si-ООС-группы ниже, чем С-ООС-группы в аналогичных пероксидах, в первую очередь за счет большей термостойкости кремнийорганической пероксигруппы. При замене Н на SCN в пероксиде одновременно несколько снижаются термостойкость и инициирующая способность. [9]
Реакции вырожденного разветвления кинетических цепей за счет возможных превращений гидроперекисных групп, образующихся при окислении макромолекул полимера и играющих основную роль при окислительной деструкции полимерных углеводородов 143 - 151, здесь, по-видимому, не имеют первостепенного значения. При окислении ПВХ в течение 100 ч в интервале 120 - 180 С в ИК-спектрах четко не проявляются характеристические частоты пероксигрупп. [10]
Характерно, что температурный коэффициент изменения скорости процесса разложения формирующихся в ПВХ пероксигрупп ( 19 7 ккал / моль) аномально низок 283 по сравнению с этим коэффициентом процесса разложения перекисных групп других озонированных полимеров, для которых энергия активации равна 30 - 35 ккал / моль. Низкую величину Егкг перекисных группировок в озонированном ПВХ следует связывать с каталитическим действием HG1, элиминирующего из полимера в ходе реакционного процесса. При этом возможно как гемолитическое, так и гетеролити-ческое ( под влиянием НС1) разложение пероксигрупп. [11]
Центральные ионы находятся в разных окислительных состояниях. Уже давно известно, что соединения этого типа имеют очень интенсивные спектры поглощения в видимой области. Известно большое число таких комплексов, причем многие из них кажутся в твердом состоянии черными, а в растворах при большом разбавлении - желтыми, зелеными или красными. Примером может служить раствор [ Ti ( H20) 6 ] 3 в 2-моляльной НС1, который нормально является пурпурно-красным. Обычно два иона металла отделены друг от друга какими-либо иными атомами, например кислородом или даже пероксигруппой, но поскольку потенциал ионизации одного иона металла точно равен сродству другого иона к электрону, имеется большая степень делокализации электрона и полосы переноса заряда смещаются к очень длинным волнам в соответствии с представлением о том, что энергия переноса близка к нулю. [12]
Страницы: 1