Пероксид - уран
Cтраница 1
Пероксид урана - осадок желтого цвета, при растворении в ярисутствии эфира в серной кислоте эфирный слой окрашивается, как и у Сг ( VI), в синий цвет. [1]
Пероксид урана может быть осажден из водных растворов иона уранила перекисью водорода. Поскольку в этих условиях осаждается обычно пероксид урана исключительно высокой чистоты, эта операция используется в крупномасштабном производстве обогащенного урана реакторного сорта. Пероксид урана не существует в безводном состоянии. Это соединение при дальнейшем нагревании или при обработке водой теряет кислород. [2]
Пероксид урана осаждается из раствора, и осадок прокаливается на воздухе в течение 30 мин при температуре около 900 С. Вес продукта после прокаливания равен 1 9931 г. Чему равен вес исходного осадка пероксида. [3]
При действии Н2О2 на раствор нитрата уранила образуется желтый пероксид урана: U02 ( NO3) 2 Н202 2Н20 - Шу 2Н20 1 2HN03 Соли уранила имеют обычно характерную желтую окраску с желто-зеленой флуоресценцией. Многие соли образуют кристаллогидраты. [4]
Пероксид урана может быть осажден из водных растворов иона уранила перекисью водорода. Поскольку в этих условиях осаждается обычно пероксид урана исключительно высокой чистоты, эта операция используется в крупномасштабном производстве обогащенного урана реакторного сорта. Пероксид урана не существует в безводном состоянии. Это соединение при дальнейшем нагревании или при обработке водой теряет кислород. [5]
На аффинажном заводе уран был подвергнут окончательной очистке осаждение. Напишите последовательно реакции, используемые для производства металлического урана, начиная с получения пероксида урана. [6]
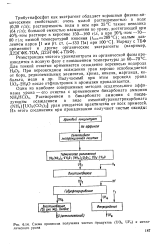 |
Схема процессов получения чистых продуктов ( UC, UF6 и металлического урана. [7] |
Реэкстракция чистого уранилнитрата из органической фазы производится в водную фазу с повышением температуры до 60 - 70 С. При переоксидном осаждении уран хорошо освобождается от бора, редкоземельных элементов, хрома, никеля, марганца, кобальта, меди и др. Получаемый при этом пероксид урана UO4 - 2H2O после отфильтровок и промывки прокаливается. [8]
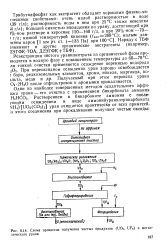 |
Схема процессов получения чистых продуктов ( UO2, UF6 и металлического урана. [9] |
Реэкстракция чистого уранилнитрата из органической фазы про - водится в водную фазу с повышением температуры до 60 - 70 С. При переоксидном осаждении уран хорошо освобождается г бора, редкоземельных элементов, хрома, никеля, марганца, ко - льта, меди и др. Получаемый при этом пероксид урана О4 - 2Н2О после отфильтровок и промывки прокаливается. [10]
Пероксид урана может быть осажден из водных растворов иона уранила перекисью водорода. Поскольку в этих условиях осаждается обычно пероксид урана исключительно высокой чистоты, эта операция используется в крупномасштабном производстве обогащенного урана реакторного сорта. Пероксид урана не существует в безводном состоянии. Это соединение при дальнейшем нагревании или при обработке водой теряет кислород. [11]
В разбавленных кислотах гидраты перекиси урана плохо растворяются. Хорошо реагируют они лишь с концентрированными кислотами, образуя растворы солей уранила. Концентрированные щелочи разлагают пероксид урана, при этом получаются нерастворимые уранаты. Ду-расова и Николаев [223] показали возможность существования сложных комплексов пероксида урана с перекисью водорода. [12]
При добавлении перекиси водорода к кислому ( 1 - 3 М Н) раствору плутония ( III), плутония ( IV) или плутония ( VI) выпадает зеленый осадок, который в насыщенном растворе иногда - бывает красно-коричневым. Осадок представляет собой пероксид плутония ( растворимые пероксидные комплексы плутония обсуждаются ниже, в разд. Уран и нептуний в четырехвалентном состоянии при добавлении перекиси водорода также образуют нерастворимые осадки, однако эти соединения, по-видимому, являются производными шестивалентного состояния, а не четырехвалентного. Пероксид урана имеет состав U04 - 2H2O, тогда как в настоящее время известно, что осадок пероксида тория, которому одно время приписывали формулу Th207, включает анионы. В этом отношении пероксид плутония более похож на пероксид тория, чем урана. Исследование показало, что в пероксиде плутоний находится в четырехвалентном состоянии. При осаждении пероксида из растворов серной, азотной или соляной кислот осадок пероксида содержит значительные количества соответствующего аниона. [13]
В разбавленных кислотах гидраты перекиси урана плохо растворяются. Хорошо реагируют они лишь с концентрированными кислотами, образуя растворы солей уранила. Концентрированные щелочи разлагают пероксид урана, при этом получаются нерастворимые уранаты. Ду-расова и Николаев [223] показали возможность существования сложных комплексов пероксида урана с перекисью водорода. [14]
Операция осаждения находит также применение при работе с макроконцентрациями плутония как на конечной стадии выделения его в производстве, так и в качестве метода очистки в лаборатории. Нерастворимые пероюсиды образуют также церий ( IV), торий и цирконий. Но эти пять пероксидных соединений осаждаются из растворов, различающихся по своей кислотности. Пероксид плутония довольно стоек в сильнокислых растворах, в то время как / пероксид урана достаточно легко растворяется в кислотах. Поэтому в процессе осаждения нероксида урана очень важно контролировать рН раствора. В табл. 10.8 приведены коэффициенты очистки осажденного плутония от различных примесей при добавке 30 % Н262 к нитратному раствору, полученному каталитическим ( с добавкой фторида) растворением плутониевого сплава. [15]
Страницы: 1