Пероксидикарбонат
Cтраница 1
Пероксидикарбонаты широко применяются как при эмульсионной, так и при суспензионной полимеризации винилфторида. [1]
Для низкотемпературной полимеризации винилфторида широко применяются пероксидикарбонаты, характеризующиеся высокими скоростями распада, обеспечивающими высокую скорость полимеризации и сокращение продолжительности процесса. [2]
В ароматических растворителях эти соединения разлагаются быстрее, чем перекись бензоила. Пероксидикарбонаты в чистом виде быстро распадаются уже при темп - pax, близких к комнатной. В связи с неустойчивостью и опасностью в обращении работа с перо-ксидикарбонатами требует принятия специальных мер предосторожности. [3]
 |
Схема процесса производства суспензионного поливинилхлорида. [4] |
Наиболее эффективными являются смеси инициаторов последовательного действия, в присутствии которых полимеризация протекает с высокой скоростью на протяжении всего процесса. Применение смеси пероксидикарбоната с порофором позволяет не только значительно повысить скорость полимеризации, но и применить более низкие концентрации инициатора, что способствует повышению термостабильности поливинилхло-рида. [5]
Суспензионный ПВХ получают по полунепрерывной схеме: полимеризация - периодический процесс, последующие операции проводятся непрерывно. В качестве инициаторов применяют растворимые в мономере динитрил азобисизомасляной кислоты, перекись лауроила, пероксидикарбонаты и др. Некоторые пероксиди-карбонаты ускоряют процесс полимеризации ВХ в 2 - 3 раза. Наиболее эффективными являются смеси инициаторов. Стабилизаторами служат метилцеллюлоза, сополимеры винилового спирта с винилацетатом и др. Водорастворимая метилцеллюлоза с содержанием 26 - 32 % метоксильных групп надежно защищает капли мономера от агрегирования при значительно более низких, концентрациях по сравнению с другими стабилизаторами. [6]
Суспензионный поливинилхлорид получают по полунепрерывной схеме. В качестве инициаторов применяют растворимые в мономере органические перекиси или азосоединения: динитрил азо - бис-изо-масляной кислоты ( порофор), перекись лауроила, пероксидикарбонаты и др. Перекись бензоила имеет более низкую активность, поэтому для промышленных целей при полимеризации винилхлорида ее ислользуют редко. Наиболее эффективными являются смеси инициаторов. [7]
Для гидроксили-рования и ацилоксилирования могут использоваться такие вещества, как арилпероксиды, ароилпероксиды, аренсульфонилперокси-ды, перкислоты и перэфиры. Одним из наиболее полезных реагентов является пероксиди ( изопропилкарбонат) ( изо - РгОСО) 2О2, дающий прекрасные выходы в сочетании с незначительным протеканием побочных реакций. Тот же пероксидикарбонат можно применять и для радикального замещения совместно с хлоридом меди при нагревании или с освещением для инициирования процесса; здесь также преобладают орто / пара-продукты. [8]
Для гидроксили-рования и ацнлоксилирования могут использоваться такие вещества, как аршшероксиды, ароилпероксиды, аренсульфонилперокси-ды, перкислоты и перэфиры. Одним из наиболее полезных реагентов является пероксиди ( изопропилкарбонат) ( ггзо - РгОСО) 2О2, дающий прекрасные выходы в сочетании с незначительным протеканием побочных реакций. Тот же пероксидикарбонат можно применять и для радикального замещения совместно с хлоридом меди при нагревании или с освещением для инициирования процесса; здесь также преобладают орго / пара-продукты. [9]
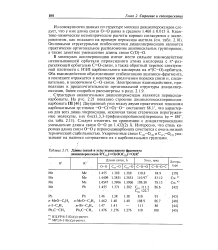 |
J. Длины Связей и углы пероксидного фрагмента диацилпероксидов R C ( ( O OOC ( 2 ( O R2. [10] |
В молекулах ацилпероксидов имеют место сильное взаимодействие несвязываюшей орбитали пероксидного атома кислорода с л - разрыхляющей орбиталъю С-О - связи, а также обратный перенос электронной плотности с НЭП карбонильного кислорода на ст ( С-О) - орбиталь. Оба взаимодействия обусловливают стабилизацию ацилокси-фрагмента, а последнее отражается в некотором увеличении порядка связи и, следовательно, в укорочении С-О - связи. Электронные взаимодействия, приводящие к предпочтительности ортогональной структуры диацилпероксидов, более подробно рассмотрены в разд. Структурно аналогичными диацилпероксидам являются пероксиди-карбонаты. Следует отметить по сравнению с диацилпероксидами уменьшение длины связи О-О до 1.432 ( 2) А. Интересно, что столь короткая длина связи О-О у пероксидикарбоната сочетается с очень низкой термической стабильностью. Укороченные связи С () - О ( 2) и С ( П - О ( Г) указывают на наличие сопряжения их с карбонильными группами. [11]
Присутствие активного наполнителя в зоне реакции полимеризации отражается на протекании всех ее стадий. Поверхность наполнителя существенным образом влияет на процесс распада пер-оксидов. В большинстве случаев присутствие развитой поверхности раздела фаз способствует ускоренному распаду пероксидных соединений по свободнорадикальному механизму. Так, в работе [418] отмечено ускорение распада гидропероксида кумола, адсорбированного на поверхности тугоплавких соединений титана. На распад бензоилпероксида и азобисизобутиронитрила влияние оказывают лишь TiC и TiC2 соответственно. С основным характером асбестового цеолита [419] связывают ускорение распада бензоилпероксида и пероксидикарбоната. [12]
Страницы: 1