Перре-нат
Cтраница 1
Перре-наты менее растворимы и термически более устойчивы, чем соответствующие перхлораты и перманганаты. Температуры плавления наиболее распространенных в анализе перренатов следующие: NaRe04 414 С, KRe04 555 С, CsRe04 616 С. Наименьшей растворимостью обладают перренаты таллия, цезия, рубидия и калия. [1]
Может содержать молибдат, перре-нат и пертехнетат. [2]
Так, при взаимодействии перре-натов с железосинеродистым калием в присутствии хлористого олова наблюдается коричневое окрашивание. Если заменить железосинеродистый калий спиртовым раствором диметилглиоксима, то появляется окрашивание от желтого до красного, а при нагревании смеси наблюдается зеленая флуоресценция; эти реакции получаются уже с 0 01 мг рения. [3]
При введении сероводорода в кислый раствор перре-ната калия выпадает черный осадок, который растворяется при действии азотной кислоты. [4]
Рений выделяют из раствора в составе перре-ната калия. [5]
Тигель с осадком высушивают до постоянного веса при 110 и взвешивают в виде перре-ната нитрона. [6]
Последние два способа применяют для получения более концентрированных растворов, из которых затем выделяют перре-наты калия или аммония, служащие исходными продуктами для производства рения. Ниже рассмотрены примеры техдологиче ских схем, в которых используются различные способы извлече-ния рения из отходов производства. [7]
Из полученного раствора, содержащего NH4ReO4 и ( NH 4) 2SO 4, после упаривания кристаллизуется перре-нат, который далее очищают перекристаллизацией. [8]
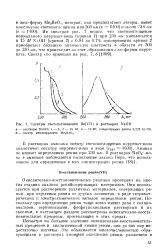 |
Спектры светопоглощения Re ( VII в растворах NaOH. [9] |
Из спектров рис. 7 видно, что светопоглощение нормального иерренат-иона ( кривая 1 при 230 нм уменьшается в 15 Ж NaOH ( кривая 2) с 0 84 до 0 74; одновременно кривая 2 приобретает большую оптическую плотность в области от 300 до 350 нм, что происходит за счет образования л езо-формы перре-ната. [10]
Еще менее устойчивы сами свободные тиокислоты. Поэтому действием сероводорода на кислый раствор перре-ната может быть легко получен черный осадок RejSr. Оба сульфида в водной среде легко окисляются до кислот НЭО. [11]
Если абсорбциометр Спеккера или подобный ему прибор отсутствует, окраску можно сравнивать в цилиндрах Несслера. Шкалу стандартов готовят из растворов, содержащих известные количества перре-ната калия, применяя те же количества кислоты, хлористого олова, роданида или диметилглиоксима. При работе по эфирному методу цилиндры Несслера неудобны. На фотоколориметрах ФЭК-М или ФЭК-Н-54 колориметрирование ведут с синим или лиловым светофильтром. [12]
Исходным соединением для получения чистого рения в большинстве случаев является перре-нат аммония. Рений, полученный из перрената калия, содержит примеси щелочных и щелочноземельных металлов, которые делают его непригодным для многих областей применения. [13]
Для разделения ионов используется различие раствори-мостей их соединений. Например, разделение молибдена и рения основано на малой растворимости молибдата кальция в воде и на достаточно большой растворимости перре-ната кальция. [14]
Неполный возгон рения при обжиге в муфельной печи может быть обусловлен частичным взаимодействием Re2O7 с кальцитом, а также окислами железа и меди с образованием перре-натов. [15]
Страницы: 1 2