Перфторизобутилен
Cтраница 2
Среди газообразных продуктов реакции может содержаться токсичный перфторизобутилен, поэтому при спуске давления в автоклаве и перегонке с паром следует соблюдать осторожность и работать под эффективной тягой. [16]
Перфторацетон 414 Перфторацетонитрил 410 Перфторвинильные соединения 414 Перфторизобутилен 412, 413 Пероторкетоны 414, 415 Пероторолефины 410 ел. [17]
При превышении предельно допустимых концентраций фтористый водород, перфторизобутилен раздражают слизистые оболочки дыхательных путей, вызывают воспалительные процессы органов дыхания, а при высоких концентрациях - отек легких. Фтористый водород обладает способностью к кунуляции. Окись углерода вызывает удушье вследствии образования карбоксигемоглобина, действует на центральную нервную систему. [18]
Большее количество воды или использование плохо высушенного растворителя приводят к гидратации перфторизобутилена. [19]
При нагревании до 80 С перфтор-у-грег-бутилпиридин вступает в дальнейшее взаимодействие с перфторизобутиленом и CsF, давая перфтор ( 2 4 6-три-грег - бутилпирид. [20]
В случаях с гексафторпропиленом можно полагать, что основной токсической примесью был перфторизобутилен. Это подтверждается материалами вскрытия и результатами патогистоло-гического исследования павших в результате острого отравления гексафторпропиленом животных. [21]
Высокая подвижность атомов фтора в а-положении сказывается в невозможности получения предельных аддуктов перфторизобутилена с обычными вторичными аминами [ К н у н я н ц, Г е р м а н, Д я т к и п, Изв. [22]
При пиролизе ( 550 - 650 С) дает тетрафторэтилен, гексафторпропилен, перфторизобутилен и гексафторэтан. [23]
При 475 С и выше основным, ответственным за токсичность, продуктом является перфторизобутилен. [24]
Синтез фторированных кетонов основан на следующих реакциях: окисление фторолефинов перманганатом калия ( например, перфторизобутилен легко окисляется в ге-ксафторацетон CFs - СО - CFs); радикальное присоединение альдегидов к фторолефинам; взаимодействие три-фторметилмагниййодида и других перфторалкильных гриньяровских реагентов с галоидными ацилами. [25]
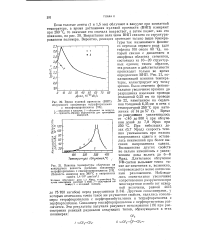 |
Время нулевой прочности ( ВНП облученного сополимера тетрафторэтилена.| Влияние температуры облучения на кажущуюся вязкость расплава сополимера. [26] |
Другими сополимерами, у которых отмечалось точно такое же улучшение свойств, являлись сополимеры тетрафторэтилена с перфторизобутиленом и тетрафторэтилена с перфторгептеном. Сополимер гексафторпропилена с перфторгептеном разлагается. [27]
При работе с этими веществами необходимо соблюдать такие же меры предосторожности, как и при работе с перфторизобутиленом. [28]
Фенил-1 1 1 -трифтор - 2 2-бис ( трифторметил) - 3 - фенилпропил-имин получают взаимодействием iN - фенилбензимидоилхлорида с перфторизобутиленом в присутствии CsF в моноглиме ( выход. [29]
Процент превращения перфторизобутилена в а-гидроперфторизомасляную кислоту можно легко увеличить, взяв в реакцию такое количество ацетона, чтобы после прибавления всего количества перфторизобутилена получился гомогенный раствор. [30]
Страницы: 1 2 3 4