Перхлорат - натрий
Cтраница 2
Перхлораты натрия и щелочноземельных металлов растворимы в этом реактиве. Избыток хлористого бария, остающийся в растворе, не мешает дальнейшему определению калия, так как перхлорат бария растворим в спирте. [16]
 |
Схема получения перхлората натрия электрохимическим окислением. [17] |
Перхлорат натрия получают электрохимическим окислением хлората натрия в растворе. Другие перхлораты обычно получают обменной реакцией перхлората натрия с соответствующими солями или нейтрализацией хлорной кислоты соответствующими основаниями. [18]
Перхлорат натрия очень гигроскопичен - даже при обычной влажности воздуха легко расплывается. Вследствие этого он неудобен для практического применения, но служит сырьем для производства других солей хлорной кислоты. [19]
Перхлорат натрия также быстро распространился в организме кролика21; перхлораты были обнаружены во всех исследованных органах через 20 мин после внутривенного вливания. [20]
 |
Растворимость NaClC4 в воде. [21] |
Перхлорат натрия хорошо растворим в воде. [22]
Если перхлорат натрия используется для последующей переработки в перхлорат аммония, необходима тщательная очистка электролизных растворов от содержащихся в них загрязнений, хтак как маточные растворы после кристаллизации перхлората аммония не могут быть, возвращены на электролиз из-за содержания в них ионов аммония. [23]
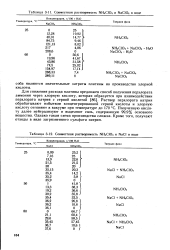 |
Совместная растворимость NH4CIO4 и NaClO4 в воде.| Совместная растворимость NH4C1O4 и NaCl в воде. [24] |
Раствор перхлората натрия обрабатывают избытком концентрированной серной кислоты и хлорную кислоту отгоняют в вакууме при температуре до 170 С. Полученную кислоту далее нейтрализуют и выделяют соль, содержащую 99 9 % основного вещества. Однако такая схема производства сложна. Кроме того, получают отходы в виде загрязненного сульфата натрия. [25]
Для перхлората натрия имеются данные до концентрации 8 М; в этой точке скорость в 20 раз меньше, чем в отсутствие соли, но линейность все еще сохраняется. Сульфат несколько увеличивает скорость, но его влияние вскоре выравнивается. Магний, кальций и лантан проявляют сильный нелинейный тормозящий эффект. [26]
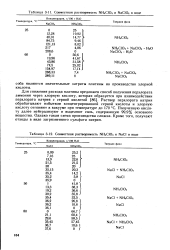 |
Совместная растворимость NH4CIO4 и NaClO4 в воде.| Совместная растворимость NH4C1O4 и NaCl в воде. [27] |
Раствор перхлората натрия обрабатывают избытком концентрированной серной кислоты и хлорную кислоту отгоняют в вакууме при температуре до 170 С. Полученную кислоту далее нейтрализуют и выделяют соль, содержащую 99 9 % основного вещества. Однако такая схема производства сложна. Кроме того, получают отходы в виде загрязненного сульфата натрия. [28]
Получение перхлората натрия возможно и непосредственно из раствора NaCl, перетекающего через каскад электролизеров. [29]
Получение перхлората натрия возможно и непосредственно из) аствора NaCl, протекающего через каскад электролизеров. [30]
Страницы: 1 2 3 4