Перхлорат - тетрабутиламмоний
Cтраница 1
Перхлорат тетрабутиламмония синтезировали в лаборатории [12] и очищали перекристаллизацией из этилаце-тата. В качестве фонового раствора может быть использован также и тетрабутиламмонийио-дид после соответствующей очистки. [1]
Если в качестве электролита используются перхлорат тетрабутиламмония, то возникает легированный полимер, в котором на один ион перхлората приходятся три молекулы пиррола. [2]
Анодное окисление пирена, перилена и азулена в тетрагид-рофуране ( ТГФ), содержащем перхлорат тетрабутиламмония. [3]
Электрохимический элемент создают путем погружения двух полос полиацетиленовой пленки в электролит и соединения каждой полосы пленки с выводами источника постоянного тока; электролитом для такого элемента служит раствор перхлората тетрабутиламмония в карбонате пропилена. При прохождении тока через такой элемент он заряжается; полиацетиленовая полоска, которая служит положительным электродом ( анодом), окисляется и легируется анионом перхлората, а полоска, которая служит отрицательным электродом ( катодом), восстанавливается и легируется катионом тетрабутиламмония. Эти ионы не подвергаются электрохимическим превращениям. Как в обычных электрохимических элементах, анионы и катионы поддерживают электрическую нейтральность системы. [4]
Например, полимерные осадки образуются на желез -: ом катоде при электрохимической сополимеризации 0 5 моль / л крилонитрила и 2 моль / л винилиденхлорида в метиленхлори - е, содержащем 0 04 моль / л перхлората тетрабутиламмония. Полученные осадки со-олимера более прочно связаны с подложкой, чем гомополимер. Однако полимерный слой не обеспечивает эффектив-ую защиту металла от коррозии. [5]
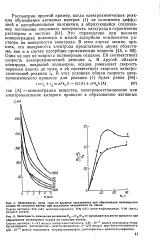
Состав раствора: 7 - 5 1 моль / л изобутилметакрилата, 2 35 10 - моль / л перхлората тетра-бутиламмония, растворитель-диметилформамид; 2 - 2 54 моль / л трег-бутилметакрилата, 2 35 Ю-2 моль / л перхлората тетрабутиламмония, растворитель - диметилсульфоксид. [7]
Анионы фонового электролита иногда оказывают существенное влияние на распределение продуктов. Если в качестве фонового электролита используют перхлорат тетрабутиламмония, ацетамидирование становится доминирующим процессом ( гл. [8]
Было найдено, что потенциал стеклянного электрода, заполненного растворами в ДМФ, изменяется на 59 мВ при изменении рН на единицу как в хлорной кислоте, так и в буферах, приготовленных из салицилата натрия и салициловой кислоты или 2 6-дихлор - 4-нитрофенола и его тетрабутилам-мониевой или натриевой соли. Диффузионный потенциал солевого моста ( 0 01 М раствор перхлората тетрабутиламмония в ДМФ), очевидно, зависит от природы и концентрации катиона в растворе. [9]
Сообщается об анодных реакциях окисления, которые ясно показывают, что тетрафторборат-ион не инертен. Эти выходы рассчитаны на прибавленный кетон в предположении, что из 1 экв. Те же результаты получены в присутствии пары электролитов: перхлората тетрабутиламмония и фторида калия. [10]
 |
Электрохимическая ячейка для обнаружения ион-радикалов методом ЭПР. [11] |
На рис. 147 представлена электролитическая ячейка, которую помещают непосредственно в резонансную кювету. Электролиз проводят на ртутном катоде при контролируемом потенциале. Для образования ион-радикалов потенциал ртутного катода поддерживают близким к потенциалу первой волны. В качестве электролита обычно используют перхлорат тетрабутиламмония в растворе диметил-формамида или ацетонитрила. Учитывая, что некоторые ион-радикалы легко взаимодействуют с донорами протонов, соль и растворитель следует тщательно обезводить. [12]
Страницы: 1