Газокинетический диаметр
Cтраница 2
Обычно при рассмотрении диффузионных данных, касающихся этой группы диффузантов, в качестве основного параметра, характеризующего их геометрические размеры, использовали по аналогии с инертными газами газокинетический диаметр. Однако поведение молекул в диффузионных процессах в газовой и конденсированных фазах принципиально различно. Несферические молекулы в газе большую часть времени находятся в свободном полете и только относительно небольшую часть - взаимодействуют друг с другом. В конденсированной полимерной фазе положение иное. Сорбированная ( растворенная) газовая молекула большую часть времени колеблется в ячейке до тех пор, пока рядом с ней не появится вакансия определенного размера, в которую молекула сможет сместиться. Для сферической молекулы безразлично, с какой стороны появится вакансия, лишь бы ее размер был равен или превышал d молекулы. Для несферической молекулы положение иное. Их форму можно аппроксимировать эллипсоидом вращения [168] с малой d и большой d ц осями. [16]
АВ, которое возбуждается перед ее фотохимическим распадом на А В-2 gi - сумма статистических весов всех электронных состояний этой молекулы, возникающих из электронных состояний нормального атома В и возбужденного атома A; d - средний газокинетический диаметр атомов А и В. [17]
Газокинетический диаметр молекулы водорода равен 2 2 - 10 - 8см и температура газа 300 К. [18]
Что касается газокинетического диаметра, то нельзя упускать из виду, что это не истинный диаметр малого шара; согласно определению это всего лишь радиус сферы покрытия при столкновениях молекул. Вследствие электрического строения атомов и молекул эта сфера покрытия определяется взаимодействием электрических зарядов сталкивающихся частиц. Таким образом, нельзя сказать, что при других методах определения размеров молекул мы получим ту же величину. В дальнейшем мы увидим, что величина 10 - 8 см приблизительно соответствует размерам области, заполненной электронами атома. Все опыты, в которых затрагивается электронная оболочка атомов, приводят к величинам такого порядка. [19]
Определяем это отношение при 0 для хлористого водорода, дипольный момент которого равен - 1 - 10 - 18 электростат. Примем г равным одинарному и двойному газокинетическому диаметру а молекулы НС1, т.е. будем рассматривать устойчивость однослойного комплекса, в котором молекулы вплотную прилегают к иону, а также двухсловного. [20]
Эти уравнения очень приближенны, так как расчеты А. Д. Степуховича имеют точность не выше одного порядка. Кроме того, не учтена разница в газокинетических диаметрах радикалов. Однако приведенный расчет показывает, что в зависимости от давления и температуры обрыв цепей при крекинге происходит в результате различных реакций рекомбинации. [21]
Экспериментальные определения вязкости позволяют найти Я, а следовательно по соотношению (VI.25) и диаметр молекулы D. В этом и состоит один из распространенных методов определения диаметров молекул, называемых иногда газокинетическими диаметрами. Другие методы основаны на измерениях теплопроводности, диффузии, а также на определении постоянной b в уравнении состояния Ван-дер - Ваальса. [22]
Так, Маскет принимает, что поскольку скорость потока пропорциональна градиенту давления и справедлив закон Дарси, проницаемость пористой среды является свойством последней, не зависящей от характеристики жидкости, которая была применена для определения проницаемости горной породы. Для пород же со сложной структурой и обладающих низкой проницаемостью величина последней при определении газопроницаемости зависит также от природы газов и газокинетического диаметра молекул, а при определении проницаемости жидкостями - от адсорбционных и электрокинетических явлений. Маскет в разделе, посвященном фильтрации под плотинами, поддерживает старую теорию Бляя. Эта теория базируется на изучении существующих гидротехнических сооружений и в настоящее время на основании работ Павловского отвергнута. [23]
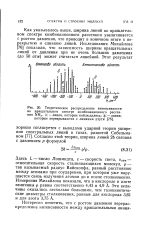 |
Теоретическое распределение интенсивности во вращательном спектре комбинационного рассеяния NH3.. X -линии, которые наблюдались. ( С - линии, которые перекрываются с линиями ртути. [24] |
Здесь L - число Лошмидта, с - скорость света, и0тн - относительная скорость сталкивающихся молекул, р - так называемый радиус Вайскопфа, равный расстоянию между атомами при соударении, при котором уже нарушается связь излучения атомов до и после столкновения. Измерения Михайлова показали, что в кислороде и азоте величины р равны соответственно 4 43 и 4 9 А. Эти величины оказались несколько большими, чем газокинетические диаметры столкновения, равные для кислорода 3 61 и для азота 3 75 А. [25]
Как ясно из предыдущего, DX... Y является межатомным расстоянием в активированном комплексе, a DAB - средний газокинетический диаметр столкновений. Y имеет более ясный физический смысл и этой величине следует отдать предпочтение. С другой стороны, энергия активации EQ относится к абсолютному нулю, а не к температуре реакции. Это различие более серьезно, но практического значения не имеет в связи с малой точностью вычисления ЕО даже в тех случаях, когда оно вообще возможно. [26]
Экспериментальные определения вязкости позволяют найти X, а следовательно, по соотношению (6.25) и диаметр молекулы D. В этом и состоит один из распространенных методов определения диаметров молекул, называемых иногда газокинетическими диаметрами. Другие методы основаны на измерениях теплопроводности, диффузии, а также на определении постоянной b в уравнении состояния Ван-дер - Ваальса. Для этого число столкновений одной молекулы А [ выражение (6.22) ] умножим на число этих молекул в 1 мл. [27]
II), передача энергии электронного возбуждения является более или менее твердо установленным фактом, пожалуй, только для растворов ароматических соединений. Данные по флуоресценции показывают, что в таких системах перенос энергии возбуждения должен происходить на расстояниях, значительно превышающих газокинетические диаметры молекул. [28]
Как видно из рисунка, п области средних скоростей ( около 30 - 80 в) полное сечение молекул более или менее близко к газокинетическому сечению. Это дает основание в тех случаях, когда учитываются все, упругие и неупругие, соударения в соответствующем интервале скоростей, вычислять свободные пробеги электронов через газокинетическое сечение молекул, иными словами, через свободный пробег молекул т, вычисленный по формулам кинетической теории газов. I ] выводятся две формулы для вычисления свободного пробега молекулы. Если все молекулы, кроме одной, считать неподвижными, то число столкновений получается следующим образом: за единицу времени молекула в среднем проходит путь v; если около этого пути как около оси ( считая путь распрямленным) построить цилиндр радиуса а, где а - газокинетический диаметр молекулы, то все молекулы, центры которых окажутся внутри этого цилиндра, испытают столкновения; число столкновений в единицу времени будет, следовательно, n a 2v, где п - число молекул в единице объема. [29]
Страницы: 1 2