Пиросульфит
Cтраница 2
При нагревании пиросульфиты разлагаются на сульфиты и SO2, а при растворении в воде гидролизуются почти наполовину с образованием гидросульфит-ионов. [16]
В растворе пиросульфит переходит в кислый сульфит. [17]
 |
Парциальное давление SO2 над Na2S2O5. [18] |
Твердый безводный пиросульфит относительно устойчив к окислению кислородом воздуха, но при влажности более 1 % он окисляется до сульфата. При нагревании в токе азота до 150 - 220 С пиросульфит натрия разлагается, причем основными продуктами разложения являются. Наряду с ними выделены в небольших количествах Na2SO4, Na2S2O3, Na2S3O6 и S8 [ 5, с. Относительное содержание каждого из этих веществ меняется в зависимости от температуры разложения. [19]
Однако, пиросульфит является значительно более ценным веществом, так как он получается в виде сухой соли Na2S2O5, выгодно отличающейся от бисульфита своей транспортабельностью. [20]
При растворении пиросульфитов в воде происходит обратная реакция. [21]
Для осаждения пиросульфита раствор 30-процентного едкого кали насыщают двуокисью серы и охлаждают до комнатной температуры. Во избежание окисления фильтрование и высушивание проводят в отсутствие воздуха. [22]
Практическое значение имеет пиросульфит, называемый также мета-бисульфит калия, применяемый в качестве восстановителя в красильном и ситцепечатном производствах и фотографии. [23]
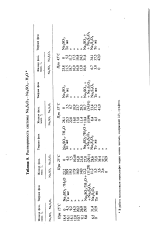 |
Растворимость системы. [24] |
В работе использовали пиросульфит марки очень чистый, содержащий 2 2 % сульфита. [25]
Сырье с добавкой пиросульфита на технически оснащенном предприятии перерабатывают без удаления консерванта, а при использовании поваренной соли его предварительно промывают в течение 10 мин в проточной воде. [26]
Сульфит, бисульфит, пиросульфит, гидросульфит и тиосульфат натрия легко окисляются ( в особенности гидросульфит) и поэтому являются хорошими восстановителями. Применение этих соединений в различных отраслях техники основано, глав ным образом1, на их восстановительных свойствах. [27]
При растворении в воде пиросульфита ( метабисульфита) натрия образуется раствор бисульфита натрия. Следовательно, ва всех случаях применения эти продукты взаимозаменимы. Однако пиросульфит является более ценным веществом, так как он получается в виде сухой соли Na2S2Os, выгодно отличающейся от бисульфита своей транспортабельностью. [28]
При растворении в воде пиросульфита ( метабисульфита) натрия образуется раствор бисульфита натрия. Следовательно, во всех случаях применения эти продукты взаимозаменимы. Однако пиросульфит является более ценным веществом, так как он получается в виде сухой. [29]
При растворении в воде пиросульфита ( метабисульфита) натрия образуется раствор бисульфита натрия. Следовательно, во всех случаях применения эти продукты взаимозаменимы. Однако пиросульфит является более ценным веществом, так как он получается в виде сухой соли Na2S2O5, выгодно отличающейся 6т бисульфита своей транспортабельностью. [30]
Страницы: 1 2 3 4