Брайтер
Cтраница 2
Бокрис и Аззам148 ш, казалось бы, установили больший, чем это отвечает тафелевской прямой, рост перенапряжения при плотностях тока вплоть до ЮОа-слГ2 и объяснили это как появление предельного тока. Однако Брайтер и Кламрот144 показали, что если построить график зависимости т) от i, получается прямая, так что не появление предельного тока, а омическое падение напряжения вызывает кажущийся рост перенапряжения. Это находится в согласии с данными Кабанова 174, по которым даже при чрезвычайно больших плотностях тока вплоть до 100 а-смг 1 выполняется тафелевское уравнение. [16]
Смит, Урбах, Харрисон и Хатфилд [307, 308] тщательно изучили хемосорбцию метанола на золотых электродах с платиновым покрытием ( ср. Результаты Брайтера и Гильмана [317] и Хазовой, Багоцкого и Васильева [318], основанные на переходных электрических характеристиках, не согласуются с данными, полученными методом меченого углерода. В широкой области потенциалов было прослежено соотношение заполнение - время: при потенциалах, превышающих 0 4 В, наблюдается тенденция к уменьшению заполнения со временем ( эффект, преимущественно связанный с медленными окислительными процессами), тогда как при потенциалах ниже 0 4 В заполнение поверхности любыми угле-родсодержащими частицами со временем растет. [17]
Наличие на кривых g f ( 9) минимума, области постоянного значения q и участка монотонного падения значений величины q свидетельствует, как это уже отмечалось в литературе, об энергетической неоднородности поверхности дисперсных осадков палладия и рутений-палладиевых сплавов. Бельд и Брайтер [7] для ряда благородных металлов также получили q, 0-кривые, ход которых свидетельствует о том, что характер адсорбции водорода резко меняется с заполнением, что может способствовать образованию различных форм связи водорода с металлом. [18]
Вопрос о том, какой потенциал соответствует состоянию, предшествующему переносу заряда в том случае, когда имеет место специфическая адсорбция, не решен до сих пор. Эта проблема была проанализирована Брайтером, Клайнерманом и Де-лахеем [10], которые рассмотрели аргументы в пользу сравнения экспериментально найденных значений Дг) с изменениями потенциала внутренней ( Acpi) и внешней ( ДФ2) плоскостей Гельм-гольца. Значения ф4 и ф2 известны для хлорида и иодида, и то лишь в первом приближении ( раздел 4, б гл. [19]
Метод единичного непрерывного наложения потенциала использован Гилманом и Брайтером в целом ряде исследований реакций анодного окисления и особенно для изучения адсорбированных частиц. [20]
 |
Влияние частоты переменного тока на величину псевдоемкости. [21] |
Долин и Эршлер [33], а также другие исследователи [61, 116] получили дополнительные сведения об адсорбции водорода на гладкой платине, использовав метод измерения емкости в переменном токе. С изменением частоты наблюдается большая дисперсия емкости, что было подтверждено в более поздней работе Брайтера [35], в которой наблюдалось два максимума ( рис. 24) при различных потенциалах. [22]
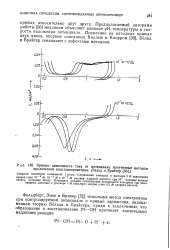 |
Кривые зависимости тока от потенциала, полученные методом циклической вольтамперометрии. ( Бельд и Брайтер. [23] |
Предполагаемый авторами работы [56] механизм объясняет влияние рН, температуры и скорости наложения потенциала. Появление на катодных кривых двух пиков, впервые описанных Биллем и Кнорром [32], Бельд и Брайтер связывают с дефектами методики. [24]
Ионизация водорода наблюдается в течение промежутка времени АВ, однако действительное количество электричества, связанное с адсорбированным водородом, соответствует заряду, пропущенному за время АВ. Аналогичным образом количество электричества, пропущенное за время DE, требуется для образования поверхностного окисла. Брайтер, Кнорр и Фелькль [22] предположили, что вторая задержка соответствует образованию законченного монослоя адсорбированного кислорода, и из величины пропущенного заряда вычислили число мест на единицу геометрической ( видимой) поверхности электрода. [25]
Измерения Пирсона и Батлера [20] можно рассматривать как первое удовлетворительное количественное определение величины водородной адсорбции на платиновых электродах, первоначально находившихся в равновесных условиях. Это позволило практически устранить ошибки, обусловленные дополнительной адсорбцией водорода из раствора, и избежать любой неопределенности, связанной с пропусканием азота через раствор. Результаты Пирсона и Батлера позднее были подтверждены Хиклингом [21], использовавшим ту же методику. Брайтер, Кнорр и Фелькль [22] расширили область этих измерений, исследовав катодно поляризуемые электроды. [26]
Результаты емкостных измерений уже приводились в раз деле 2 6 этой главы; рис. 61 и 62 иллюстрируют влияние адсорбции ионов хлора. Кривые дифференциальной емкости на рис. 61 заметно изменяются с концентрацией соляной кислоты, пока она не превышает 10 - 4 М; дальнейшие изменения невелики. Согласно Брайтеру [111], при этой концентрации достигается состояние, близкое к насыщению. [27]
Вначале будет рассмотрен первый метод с использованием кривых заряжения. В этом методе находящийся на поверхности электрода атомарный водород окисляется до Н 1 при пропускании анодного постоянного тока ia, причем его количество можно определять из затраченного количества электричества н, используя закон Фа-радея. Это было установлено различными авторами, исследовавшими данный вопрос. Первые такие измерения были проведены Боуденом 313 и Батлером и Армстронгом 314 на гладкой платине. В последующих работах Батлером, Армстронгом и Пирсоном318 316, Фрумкиным, Эршлером, Шлыгиным и Дебориным 317 - 319 и Хиклингом 320 324 была исследована гладкая платина; Фрумкиным, Шлыгиным и Эршлером 162 319 321 322 - платинированная платина; Дебориным и Эршлером 323 - золото; Фрумкиным, Аладжаловой и Федоровой 140 325 - палладий и Брайтером, Кнорром и Фельклем 236 - платина, иридий, родий и золото. [28]
Здесь рассматривается только анодное окисление водорода. Кинетика этой реакции описана в обзорах Феттера [176] и Фрумкина [3] и поэтому подробно не обсуждается, тем более, что для нас представляет интерес в первую очередь ингибирование хемосорбированным кислородом. Следует контролировать диффузию водорода, растворимость которого мала, и вносить на нее поправку. Снижение тока вызвано вначале специфической адсорбцией анионов, а при более высоких анодных потенциалах-хемосорбированным кислородом. В этом случае наблюдается очень сильное торможение. Подробно этот последний случай изучил Брайтер [59], который обнаружил гистерезис на кривых зависимости тока от потенциала, полученных при непрерывном изменении потенциала. [29]
Страницы: 1 2