Рассматриваемое пламя
Cтраница 1
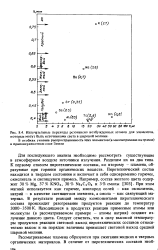 |
Излучательные переходы резонансно возбужденных атомов для элементов, которые могут быть источниками света в шаровой молнии. [1] |
Рассматриваемые пламена образуются при сжигании жидких и твердых органических материалов. [2]
В рассматриваемых пламенах образуется очень мало Н2СО, - причем он быстро вступает в реакцию с другими радикалами. [3]
 |
Горячие диффузионные пламена ( по Бурке и Шуману [ 4661. [4] |
Следовательно, в случае рассматриваемого пламени разогрев не превышает нескольких градусов. [5]
Такое разделение не отражает основных физических особенностей излучения рассматриваемых пламен. Любое пылеугольное пламя следует рассматривать как полусветящееся пламя, так как наиболее характерная особенность такого пламени, отличающая его от пламени газа и жидкого топлива, связана с излучением твердых золовых и коксовых частиц, размеры которых обычно превышают основные длины волн теплового излучения пламени. [6]
Энергия, выделяющаяся в этом процессе, является основным источником излучения рассматриваемых пламен. [7]
Включение молекул М2 в механизм реакций М Х2 необходимо также и потому, что при низком давлении, когда тройные соударения весьма мало вероятны, взаимодействие атома галоида, возникающего в этой реакции ( см. ниже), с атомом металла возможно только на стенках реакционной трубки; следовательно, люминесценцию, которая наблюдается L объеме реакционной зоны, нельзя отнести за счет реакции М X - МХ. Как мы увидим ниже, энергия, выделяющаяся в этом процессе, является основным источником излучения рассматриваемых пламен. [8]
Внутри зоны голубого свечения на спектр НСО накладываются полосы СЬЫ), интенсивность которых ослабевает с приближением к границам; горячих пламен. Для объяснения одновременного появления холоднопламенного свечения и нормального сгорания предполагается затухание горячего пламени, вследствие охлаждения в ходе расширения, закалка пламени у стенок, распределение в объеме под действием завихри-вания - различных стадий воспламенения. Однако сама характеристика рассматриваемых пламен, как нормального горячего воспламенения, не соответствует наблюдаемому повышению давления. [9]
Конечно, такой подсчет лишь грубо ориентировочный, так как скорость детонации, например, с повышением начальной температуры смеси уменьшается, температура же в наших условиях выше принятой в указанном расчете Зельдовича. Кроме того, в нашем случае процесс развивается в частично прореагировавшей смеси. И все же этот расчет указывает на малую глубину химического превращения во фронте рассматриваемого пламени ( так как в противном случае волна самовоспламенения должна была бы распространяться с большей скоростью), после прохождения которого заряд должен содержать еще значительную долю невыделившейся энергии сгорания. [10]
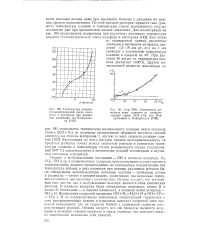 |
Температура пламени стехиометрической смеси водорода и кислорода при различных давлениях ( по Кондратье-ву [ ИЗ ]. [11] |
Наряду с возбужденными частицами - ОН в пламени водорода, О2, СО2, ОН и др. в пламени окиси углерода, присутствующих в зоне горения в концентрациях, намного превосходящих их равновесные концентрации при температуре пламен, в этих пламенах при помощи различных методов были обнаружены невозбужденные активные частицы - свободные атомы и радикалы - также в концентрациях, значительно ( на несколько порядков величины) превышающих равновесные. Отсюда следует, что источником этих частиц, как и возбужденных молекул, является сама химическая реакция. В пламени водорода были обнаружены гидроксил, атомы Н и атомы О ( последние - в горячих пламенах), в пламени окиси углерода - ОН и О. Вычисления скоростей процессов ОН Н2 Н2О Н и ОН СО СО2 Н из непосредственно измеренных концентраций гидроксила в зоне рассматриваемых пламен и известных констант скоростей этих процессов показывают, что их скорости близки к суммарной скорости соответствующих реакций. Отсюда следует, что эти процессы являются ведущими в реакциях горения водорода и окиси углерода, что вытекает также из химического механизма этих реакций. [12]
 |
Комбинированная система распылитель - горелка. [13] |
В качестве растворителя проверены бензол, толуол, гек-сан и октан. Расчетным путем установлена максимальная температура пламен бензола, толуола, гексана и октана с воздухом: 2200; 2220; 2040 и 2080 К соответственно. Полученные данные свидетельствуют о том, что по температуре и составу продуктов сгорания бензольное и толуольное пламена занимают промежуточное положение между ацетиленовым и пропан-бутановым пламенами. Гексановое и октановое пламена по своим свойствам близки к пропан-бутановому. Относительное расположение значений температур пламен хорошо коррелирует с энтальпией топлив. Гексановое, октановое ипро-пан-бутановое пламена в ряду рассматриваемых пламен имеют наименьшую температуру вследствие того, что распад молекул этих топлив сопровождается поглощением тепла, в то время как при распаде молекул ацетилена, бензола и толуола, наоборот, выделяется тепло. [14]
Реакция атомов щелочных элементов с галогенами имеет ряд особенностей. Так, выход света в этих реакциях при повышении температуры уменьшается. Полани и Шай [460], отрицательный температурный коэффициент выхода света в реакции Na - г С12 соответствует энергии 18 5 ккал, близкой к энергии диссоциации молекулы Na2, равной3 17 5 ккал. Включение молекул М2 в механизм реакций М Х2 необходимо также и потому, что при низком давлении, когда тройные соударения весьма маловероятны, взаимодействие атома галогена, возникающего в этой реакции ( см. ниже. Отсюда видно, что концентрация молекул Na2 в разреженном пламени достаточно велика, чтобы с реакцией атомов галогена с молекулами М2 не только нужно было считаться, но и признать ее основным гомогенным процессом. Энергия, выделяющаяся в этом процессе, является основным источником излучения рассматриваемых пламен. [15]
Страницы: 1 2