Браунмиллерит
Cтраница 1
Браунмиллерит в СаС12 в отличие от трехкальциевого алюмината затворяется и твердеет нормально, но затем прочность резко падает. [1]
Браунмиллерит С4АР при 120, 160 и 200 С твердеет в воде и в ЫаС1 с быстрым ростом начальной прочности. Начальная прочность камня С4АР в воде и в МаС1 значительно выше, чем у С3А, а прочность камня С4АР в ЫаС1 при 120 и 160 С снижается медленнее. [2]
В Ыа2804 браунмиллерит ( С4АР) твердеет нормально, достигая при 20 С за 90 сут 43 МПа. Затем прочность резко падает до 3 2 МПа; при 70 С картина та же, только спад наступает раньше - к 60 сут. Камень С4АР в Ма2804 состоит сначала из С4АН1з, к 60 сут образуется ЗГСАК, к 120 сут - гипс, ГСАК, ГСФ и АН. Спад прочности к 90 сут связан с распадом ЗГСАК на ГСАК, гипс и АН; это хорошо подтверждает и отрицательная контракция. [3]
Образование одного из основных соединений портландцемент-ного клинкера - минерала браунмиллерита 4СаО - А12Оз - Ре2Оз, как показывают результаты многочисленных исследований, также-протекает ступенчато. [4]
Для растворения трехкальциевого алюмината употребляется, раствор азотной кислоты, для браунмиллерита 4СаО А120з Fe203 - раствор соляной кислоты / а для кальциевых силикатов и портландцемента-смесь растворов азотной и плавиковой кислот. [5]
Большая скорость химических реакций портландцемента с водой связана с высокой степенью термодинамической неустойчивости содержащихся в нем минералов ( алита, белита, трехкильциевого алюмината браунмиллерита) по отношению к продуктам их реакций с водой. [6]
В смесях, где соотношение А12Оз: Fe2O3l 38, Fe2O3 уже в эвтектической точке при 1338 полностью перейдет в состав жидкой фазы, и весь браунмиллерит при 1338 будет расплавлен. [7]
 |
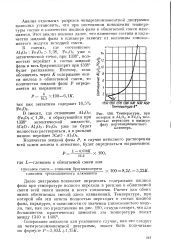
Светопреломление твердых растворов 2СаО Ре20э - 4СаО Al203 - Fe203. [8] |
В 1937 г. Мерков, Шишаков и Торопов, в результате рентгенографического и кристаллооптического изучения системы 4СаО - А130з Р203 - 5СаО А1аОз, показали, что браунмиллерит образует твердые растворы не только с ферритами, но и с алюминатами кальция, растворяя, например, в своей кристаллической решетке до 30 % 5СаО ЗАЬОз. [9]
 |
Температуры, при которых и А12О3 и Fe20s полностью переходят в жидкую фазу портландцементного клинкера. [10] |
В смесях, где соотношение АЬОз: Ре20з 1 38, Fe203 уже в эвтектической точке, при 1338, полностью перейдет в состав жидкой фазы и весь браунмиллерит при 1338 будет расплавлен. [11]
Последний далее реагирует с избыточной свободной окисью кальция, образуя при этом 5СаО - ЗА12Оз и ЗСаО-А12Оз и только при температурах в 1100 - 1200 идет взаимодействие между ферритами и алюминатами кальция, приводящее к образованию браунмиллерита. [12]
Основными клинкерообразующими минералами являются ЗСаО S102 - трехкальциевый силикат или алит; 2CaO - SiO2 - двухкальциевый силикат или белит; ЗСаО А Оз - трехкальциевый алюминат или целит и 4СаО - AlaOs-F Os - четырехкаль-циевый алюмоферрит или браунмиллерит. [13]
Последний затем реагирует с избы - - точной свободной окисью кальция, образуя при этом 5СаО ЗАЬОз и ЗСаО AlaPs и только при температурах 1100 - 1200 идет взаимодействие между ферритами и алюминатами кальция, приводящее к образованию браунмиллерита. [14]
По мере повышения температуры до 1200 С этот твердый раствор связывает все большее количество СаО и превращается в двухкальциевое соединение, твердый раствор С2А - C2F, или 2СаО - ( Аж - Р Ь Оз. В портландцементе промышленного производства этот твердый раствор содержит примерно поровну оксиды алюминия и железа. Минералогическое название его браунмиллерит, чаще называют его четырехкальциевым алюмо-ферритом. [15]
Страницы: 1 2