Пластохинона
Cтраница 3
О природе его мы почти ничего не знаем; считается, что он сходен с реакционным центром Р700 фотосистемы I, т.е. тоже представляет собой комплекс хлорофилла с белком. Мало что известно и о природе первого переносчика электронов в этой цепи; обычно его обозначают как Z. От восстановленной формы Z электроны передаются вниз к пластохинону, или PQ ( рис. 23 - 13) - жирорастворимому хи-нону с длинной изопреноидной боковой цепью, напоминающему убихинон дыхательной цепи митохондрий. От него они переходят на цитохром / ( от лат. Цитохром / передает электроны медьсодержащему голубому белку-пластоцианину. [31]
В природных источниках ( главным образом, в растениях) чаще всего они встречаются в виде фенольных или изо-преноидных производных. Орто-хиноны встречаются значительно реже, чем пара-хиноны. Из производных бензохи-нона, в первую очередь, следует отметить две серии веществ: пластохиноны и убихиноны, очень близкие по структуре и по биологическим функциям. [32]
Общая картина такова, что при переносе электронов от донора на акцептор фотосистемой I образуется сильный восстановитель, который может восстанавливать NADP до NADPH, и слабый окислитель, который тем не менее способен получать электроны от пластоцианина. Вместе с тем перенос электронов с донора на акцептор фотосистемой II приводит к образованию сильного окислителя ( окисленный донор), который может осуществлять окисление воды и выделение кислорода. Образующийся при этом восстановитель ( восстановленный акцептор), хотя и более слабый, чем в фотосистеме I, достаточно силен для передачи электронов через последовательность компонентов пластохинон - цитохром f - пластоцианин. [33]
Как было указано выше, и-дифенол - гидрохинон может служить донором электронов в цитохромоксидазной системе, о-дифе-нол - пирокатехин - не может. Но хинон, образующийся из последнего, способен окислять восстановленный цитохром С, а хинон, полученный из гидрохинона-не способен. Все это является иллюстрацией различия поведения фенолов в процессах окисле ния. В свободной форме фенолы ( кроме пластохинона) в организмах не обнаружены, они находятся в форме различных производных. Пирока-техиновый фрагмент содержится в кофейной и хлорогеновой кислотах, широко распространенных в растениях. Флороглюцино-вый фрагмент встречается в молекулах флавоноидов. Из хлоропла-стов растений, выделено вещество, названное пластохиноном. Подобные вещества найдены и в животных организмах. В большинстве исследований в области биологического окисления использовались простые, обычно несвойственные организмам фенолы. В связи с этим возникает вопрос, в какой мере результаты опытов, проведенных с этими веществами, могут отражать процессы, протекаемые в живых организмах. [34]
Рядом работ показано, что способность хлоропластов осуществлять реакцию Хилла зависит от наличия в них пластохинона. При экстракции хлоропластов петролейным эфиром, гептаном, изо-октаном они теряют способность восстанавливать на свету KjFeCciOg, бензохинон, НАДФ. Эту потерю фотохимической активности хлоропластов вначале объясняли удалением из них / 3-каротина ( i yBCh, French1957) Однако последующие опыты с добавлением очищенного р - каротина показали, что он не восстанавливает способности к реакции Хилла. Шло доказано, что потеря фотохимической активности хлоропластов, экстрагированных петролейным эфиром, обусловлена извлечением из них пластохинона. [35]
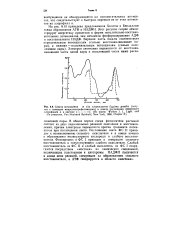 |
Спектр поглощения in situ хлоропластов Euglena gracilis ( получен с помощью микроспектрофотометрии и спектр поглощения очищенного. [36] |
В общих чертах схема фотосинтеза растений состоит из двух параллельных реакций окисления и восстановления, причем электроны переносятся против градиента потенциала при поглощении света. Поглощение света ФС II приводит к возникновению сильного окислителя и в конце концов к образованию молекулярного кислорода и слабого восстановителя. Фотопроцесс в ФС I приводит к генерации сильного восстановителя и сопутствующего слабого окислителя. Слабый восстановитель из ФС II и слабый окислитель из ФС I сопрягаются посредством мостика из химических соединений, включающих пластохинон и цитохромы. [37]
В результате изменяется восстановительный потенциал. Как акцептор электронов в световой системе II выступает пластохинон, диметилированное производное бензохинона. От пластохинона электроны через множество промежуточных стадий поступают к цитохрому / - железосодержащему протеиду. Затем следует световая реакция I, поднимающая электроны на ступень с восстановительным потенциалом - 0 4 В и далее к ферредоксину, а оттуда к пластохинону, через цитохром / и снова к хлорофиллу. [38]
 |
Схема тилакоида по Кальвину. [39] |
По строению ламеллы гран сходны с мембранами оболочки и стромы. Различие состоит главным образом в том, что в ламеллах гран один из слоев липидов в бимолекулярном слое замещен мономолекулярным слоем пигментов. Кроме того, в ламеллах тилакоид обнаружены регулярно повторяющиеся субъединицы - квантосомы, имеющие форму сплющенной сферы диаметром 180X160 А и толщиной 100 А. Каждая такая частица, помимо белка и липидов, содержит 230 молекул хлорофилла ( 160 - хлорофилла а и 70 - хлорофилла Ь), 48 молекул каротиноидов, цитохромы, пластохиноны, ферредоксин, марганец, медь. [40]
Пластохинон А; преобладающий в хлоропластах шпината, имеет структуру, изображенную на рис. 10 - 8, с девятью изопреноидными звеньями в боковой цепи. В хлоропластах шпината присутствует по меньшей мере шесть других пластохинонов. Особенно широко распространены пластохиноны С, гид-роксилированные в различных положениях боковой цепи. В пластохи ноне В эти гидроксильные группы ацилированы. Таким образом, в цепи переноса электронов может функционировать одновременно несколько разных пластохинонов. По имеющимся оценкам, на каждый реакционный центр приходится около пяти молекул пластохинонов, так что пластохиноны могут служить своего рода электронным буфером между двумя фото-синтезирующими системами. [41]
Страницы: 1 2 3