Восстановленная платина
Cтраница 1
Восстановленная платина полностью осаждается на волокне. Таким путем удается приготовить массу с содержанием 2 % платины, но очень активную, могущую на 1 AT платины дать от 600 до 700 кг SOs в сутки. [1]
Нагревают до тех пор, пока раствор над осадком восстановленной платины станет совершенно бесцветным, что свидетельствует о полноте восстановления. Раствор взбалтывают с небольшим количеством СаСОз для нейтрализации образовавшейся НС1, фильтруют, промывают осадок на фильтре горячей водой. [2]
Вещества Д1 и Д2 имеют один и тот же молекулярный вс-с М 126 и при селективном гидрировании над восстановленной платиной в кислой среде образуют одно и то же карбонильное соединение ( М 128), которое дает положительную иодоформенную пробу Определите строение и стереохимию соединений Д1 и Дг и объясните спектральные данные, гр вгдеипыс ниже. [3]
По-видимому, данный вопрос представляет для нас лишь чисто академический интерес, так как наши опыты по перераспределению дейтерия между дейтерированным бензолом и бензолом, а также другими многоядерными углеводородами на предварительно восстановленной платине показали, что при этом преобладающую роль играет механизм диссоциативного я-комплексного замещения. Очень интересно отметить результаты, изложенные в докладе 25, где найдено, что некоторые реакции перераспределения быстро протекают на напыленных металлических пленках, и тем самым подтверждена преимущественная роль диссоциативного механизма. [4]
Для точного определения суммы калия и натрия и каждого из них в отдельности ( контрольные анализы, анализы исследовательского характера) следует предпочесть отделение кальция и магния спиртово-аммиачным раствором углекислого аммония, удаление солей аммония, определение суммы хлоридов калия и натрия ( если в соли есть сульфат-ион, то он должен быть удален до отделения щелочноземельных металлов) и определение калия хлороплатинатным методом со взвешиванием восстановленной платины. [5]
Можно также вводить раствор хлороплатината калия небольшими порциями в 10 мл кипящего 20 % - ного раствора формиата натрия, кипятить 15 - 20 мин. После этого восстановленная платина легко оседает на дно. Раствор над осадком должен быть бесцветным и прозрачным. [6]
Следят за тем, чтобы весь магний растворился. Если выпадают основные соли магния, то снова подкисляют соляной кислотой и кипятят. Осадок восстановленной платины отфильтровывают, промывают водой; последние промывные воды не должны давать помутнения от добавления раствора AgNOs. Промытый осадок высушивают, прокаливают, охлаждают и взвешивают. [7]
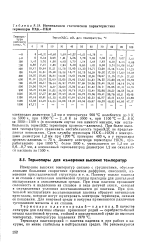 |
Номинальная статическая характеристика термопары НХК-НКМ. [8] |
Поэтому только платина и ее сплавы с металлами платиновой группы пригодны для длительной эксплуатации в окислительных средах. При этом платина проявляет склонность к выделению из сплавов в виде летучей окиси, которая в определенных условиях восстанавливается до платины. При длительной эксплуатации восстановленная платина образует нитевидные кристаллы, которые могут шунтировать электроды термопары, снижая ее показания. Для инертной среды и вакуума применяются различные тугоплавкие металлы и их сплавы. [9]
Определение калия в виде хлороплатината калия в упрощенной Ф р е з е н и-у с о м форме прежде было общепринято. Оно основывается на нерастворимости хлороплатината калия в чистом спирте. Растворимость этой соли увеличивается с разведением спирта. Наибольшее внимание следует обращать на абсолютную чистоту хлорной платины, особенно если она приготовлена из восстановленной платины, как это прежде практиковалось в заводских лабораториях. В остальном осадок хлороплатината калия обрабатывается так же, как и в случае перхлоратного метода. [10]
Хорошими сероустойчивыми катализаторами являются сульфиды молибдена и вольфрама. С повышением температуры, однако, активность сульфидных катализаторов резко возрастает, и в условиях деструктивной гидрогенизации они оказываются активнее, чем Pt и Pd. Если скорость гидрирования над восстановленным Pd при 100 в 100 раз превышает скорость гидрирования над сернистым молибденом, то при 450 сернистый молибден в 13 раз активнее палладия. Изучение сравнительной активности гидрирующих катализаторов проводилось Л. С. Альтманом и М. С. Немцовым, которые пришли к выводу, что энергия активации, а следовательно, и температурный коэффициент скорости реакции, значительно выше при гидрировании над сульфидами молибдена и вольфрама, чем над восстановленной платиной, палладием или никелем. Поэтому повышение температуры сказывается на активности этих двух групп катализаторов по-разному. [11]
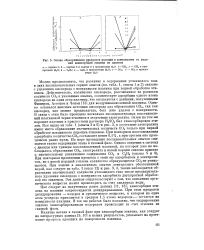 |
Состав образующихся продуктов реакции в зависимости от условий хемосорбции этилена на платине. [12] |
Можно предположить, что различие в содержании углекислого газа в двух последовательных сериях опытов ( см. табл. 1, опыты 1 и 2) связано с удалением кислорода с поверхности платины при первой обработке этиленом. Действительно, количество кислорода, рассчитанное из разности количеств С02 в указанных опытах, соответствует адсорбции одного атома кислорода на один атом платины, что согласуется с данными, полученными Фишером, Астоном и Чоном [15] для воздушноокисленной платины. Однако оставался неясным источник кислорода для образования С02, так как кислород, как можно предполагать, был уже удален с поверхности. В связи с этим было проведено несколько последовательных восстановлений платиновой черни этиленом в отсутствие электролита. Затем на том же порошке платины в присутствии раствора H2S04 был хемосорбирован этилен. Как видно из табл. 1 ( опыты 3 и 6) и рис. 3, в отсутствие электролита имеет место образование значительных количеств С02 только при первой обработке платинового порошка этиленом. При повторном восстановлении адсорбента количество С02 составляет менее 0 1 %, а при третьем оно практически равно нулю. По мере проведения последовательных опытов снижается также содержание этана в газовой фазе. Однако введение в систему с дважды или трижды восстановленной платиной, на которой уже не наблюдалось образование С02, электролита и новой порции этилена привело к значительному увеличению содержания С0а и С2Нв ( опыты 5 и 9), При повторном проведении процесса с теми же адсорбентом и электролитом, но с новой порцией этилена количество образующегося С02 не уменьшается. При замене в аналогичных опытах электролита обезгаженной водой, как следует из табл. 1 ( опыт 12) и рис. 3, б, также наблюдается образование значительных количеств углекислого газа после предварительного удаления кислорода с поверхности адсорбента двухкратной обработкой его этиленом. Эти данные свидетельствуют о том, что окисление органического вещества может происходить за счет кислорода воды. [13]
Страницы: 1