Пленка - водород
Cтраница 2
В этих случаях нагреваемая деталь является катодом. Поверхности детали, соприкасающиеся с электролитом, обволакиваются пленкой водорода, что увеличивает сопротивление. Поэтому при прохождении тока выделяется значительное тепло, нагревающее деталь. [16]
Вначале полагали, что хорошие свойства были получены благодаря чрезвычайно совершенной технике напыления, но работы В. Пауля и другие работы показали, что это связано с присутствием в пленках водорода. Водород в a - Si: H уменьшает плотность состояний дефектов благодаря компенсации оборванных связей. [17]
Если включить элемент на внешнюю цепь, то электроны из цинкового электрода станут переходить в медный и нейтрализовать на нем водородные ионы. В результате нейтрализации образуются молекулы водорода, которые сначала тонким слоем покрывают медный электрод, а затем выходят из электролита в виде газа водорода. Медный электрод, покрытый пленкой водорода, превращается как бы в водородный электрод с потенциалом, равным нулю ( табл. 19), вследствие чего разность потенциалов на зажимах элемента после его непродолжительной работы снижается до 0 7 в. Для устранения поляризации применяют химические деполяризаторы - вещества, богатые кислородом. Соединяясь с водородом, кислород образует воду и этим самым исключает образование пленки на электроде. [18]
Один стержень был стеклянный, а другой - алюминиевый. Поскольку алюминий проявляет тенденцию к растворению в воде, на его поверхности могут оставаться пленки водорода, неподдающиеся удалению при предварительном воздействии давления. [19]
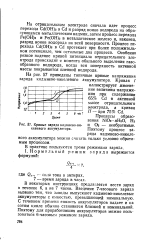 |
Кривые заряда кадмиево-никелевого аккумулятора. [20] |
На отрицательном электроде сначала идет процесс перехода Cd ( OH) a в Cd и разряд ионов водорода на образующемся металлическом кадмии, затем процесс перехода Ре ( ОН) з и Fe ( OH) a в металлическое железо и, наконец, разряд ионов водорода на всей поверхности. Процесс перехода Cd ( OH) a в Cd протекает при более положительном потенциале, чем остальные два процесса. Особенно резкое падение кривой потенциала отрицательного электрода происходит с момента обильного выделения газообразного водорода, когда вся поверхность активной массы покрывается пленкой водорода. [21]
Химическая очистка может оказаться очень эффективной и экономичной, но ее можно применять только, хорошо зная действие химических веществ на качество воды. Например, хлорированные углеводороды могут дать воде привкус и запах и могут быть вредны для потребителей и для водопроводных устройств; медный купорос не принесет пользы при высокой щелочности воды, а хлор может оказаться не эффективным в открытой воде, вследствие влияния солнечных лучей. Успешно можно применять кислоты, особенно при очистке труб небольшого диаметра для удаления отложений углекислого кальция при условии добавки к кислоте ингибитора. Пленка водорода, удерживаемая ингибитором, защищает металл от действия кислоты, в то же время ингибитор не тормозит действия кислоты на отложения кальция. [22]
Другой участок поверхности металла, который имеет более положительный электродный потенциал, в контакте с электролитом становится катодом. Например, при наличии кислот в электролите на катодном участке металла ионы водорода поглощают избыток электронов и тем самым разряжаются, превращаясь в атомы водорода. Атомы водорода, соединяясь друг с другом, могут образовывать молекулы водорода, а они в виде пузырьков газа выделяются из раствора. Однако, атомарный водород может образовывать оболочку на поверхности катода, и эта оболочка тормозит коррозионный процесс вплоть до его прекращения. Образование оболочки - пленки водорода называют поляризацией. Обратный процесс - разрушение водородной пленки, связанный с удалением водорода с поверхности катода, называют деполяризацией, а вещества, способные связывать и удалять водород, называют деполяризаторами. [23]
Другой участок поверхности металла, который имеет более положительный электродный потенциал, в контакте с электролитом становится катодом. На катоде происходит, ассимиляция тех электронов, которые освободились на анодном участке металла. Например, при наличии кислот в электролите на катодном участке металла ионы водорода поглощают избыток электронов и тем самым разряжаются, превращаясь в атомы водорода. Атомы водорода, соединяясь друг с другом, могут образовывать молекулы водорода, а они в виде пузырьков газа выделяются из раствора. Однако, атомарный водород может образовывать оболочку на поверхности катода, и эта оболочка тормозит коррозионный процесс вплоть до его прекращения. Образование оболочки - пленки водорода называют поляризацией. Обратный процесс - разрушение водородной пленки, связанный с удалением водорода с поверхности катода, называют деполяризацией, а вещества, способные связывать и удалять водород, называют деполяризаторами. [24]
На участках без блуждающих токов широко применяются заземляющие электроды с использованием медного купороса. Значительное расхождение в разности напряжения наблюдается между стальными и мед-нокупоросными электродами, когда оба находятся в контакте с одной и той же почвой или водой. В случае прокоррозированного железа отрицательный потенциал может быть равен 0 20 в по отношению к меднокупоросному электроду. Потенциал анодных поверхностей достигает 0 80 в. Если электрическим способом довести отрицательный потенциал трубы до 0 85 в по отношению к меднокупоросному электроду, то скорость коррозии будет ничтожно мала. При таком напряжении местные катоды на поверхности трубы покрываются пленкой водорода, и стенание тока с трубы в почву снижается до нуля. Потенциалы трубы менее 0 85 в и отрицательные потенциалы по отношению к меднокупоросному электроду свидетельствуют о том, что незначительная коррозия может произойти. [26]
Страницы: 1 2
