Окисная гидроокисная пленка
Cтраница 1
Окисные и гидроокисные пленки, образующиеся на магниевом электроде, при наличии воды или влажного воздуха оказываются легко проницаемыми для ионов хлора и сульфат-ионов. По этой причине магниевые электроды не подвергаются сильной поляризации. [1]
Защитные окисные и гидроокисные пленки, которые образуются на аноде, подверженном действию воды или влаги, легко разрушаются хлоридными и сульфатными ионами. Прохождение электрического тока через продукты растворения магниевого анода сопровождается незначительной поляризацией, пока прилежащая среда содержит достаточное количество анионов. [2]
Электронографичеекое иссле дование окисных и гидроокисных пленок на металлах. [3]
Расчеты показывают, что образование окисных и гидроокисных пленок почти на всех металлах становится возможным еще до достижения потенциала, необходимого для разряда ионов гидроксила. [4]
Причиной наступления локальной пассивности является образование окисных и гидроокисных пленок. [5]
Дан ков, Игнатов Д. В. и Ш ишаков Н. А. Электронно-графические исследования окисных и гидроокисных пленок на металлах. [6]
В настоящей книге речь идет только о работах по исследованию окисных и гидроокисных пленок на металлах. [7]
Этот период замедленного действия принято называть взводимостью или периодом активации, который вызывается постепенным удалением с поверхности магния окисных и гидроокисных пленок. [8]
В зависимости от природы металла и электролита, а также параметров режима на поверхности полируемого металла могут протекать такие процессы: образование вязкой пленки, переход ионов металла в электролит, наступление пассивного состояния, выделение кислорода, образование окисных и гидроокисных пленок. [9]
Для снятия жировых, окисных и гидроокисных пленок и прочих посторонних загрязнений применяют электролитическую полировку и промывку в различных средах. [10]
На качество промывки существенно влияет ее продолжительность. Слишком продолжительная промывка приводит к образованию на металле окисных и гидроокисных пленок, что может неблагоприятно сказаться на прочности сцепления покрытия с основой. Хотя промывка - простая операция, это не снижает ее значения в общем технологическом процессе нанесения покрытий. [11]
Необходимо подчеркнуть, что образование защитных слоев на меди наблюдается задолго до достижения потенциала выделения кислорода, поскольку прежде всего на электроде ( аноде) будут протекать реакции с более отрицательным потенциалом. По мере сдвига потенциала в положительную сторону начинают протекать реакции 5 и 6 ( табл. 19), приводящие к возникновению на электроде окисных и гидроокисных пленок. [12]
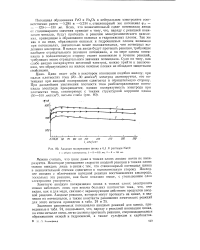 |
Анодная поляризация цинка в 0 1 N растворе NaCl. [13] |
Потенциал образования FeO и Fe203 в нейтральном электролите соответственно равен - 0 280 и - 0 234 в, стационарный же потенциал фст - 120ч - 130 мв. Ясно, что незначительный сдвиг потенциала анода от стационарного значения приведет к тому, что, наряду с реакцией ионизации металла, будут протекать и реакции электрохимического окисления, приводящие к образованию окисных и гидроокисных пленок. Так же как и на меди, образование окисных и гидроокисных пленок возможно при потенциалах, значительно менее положительных, чем потенциал выделения кислорода, В начале на аноде будут протекать реакции, требующие наиболее отрицательного значения потенциала, а по мере сдвига потенциала в положительную сторону станет возможным и течение реакций, требующих менее отрицательного значения потенциала. Судя по тому, как слабо анодно поляризуется железный электрод, можно прийти к заключению, что образующиеся на железе окисные пленки не обладают защитными свойствами. [14]
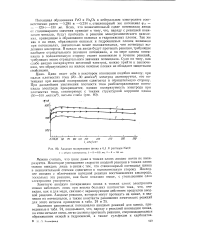 |
Анодная поляризация цинка в 0 1 N растворе NaCl. [15] |
Страницы: 1 2