Плотность - кислота
Cтраница 3
 |
Измерение плотности электролита. [31] |
По табл. 28 находим, что при плотности кислоты 1 225 г / см3 в 1 л должно содержаться 0 373 кг кислоты. [32]
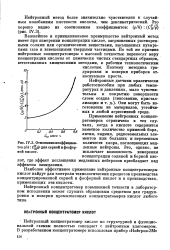
Следования Вайнела по изучению зависимости емкости of плотности кислоты воспроизведены графически на рис. 48, из которого следует, что емкость аккумуляторов возрастает по мере увеличения плотности кислоты. [33]
 |
Схема приготовления раствора серной кислоты. [34] |
Кислоту для регенерации отмеривают по объему, причем плотность кислоты определяют плотномером или ареометром. [35]
Расход кислоты на очистку составляет 4 %; плотность кислоты при 45 С Q45 1800кг / л13; время, затрачиваемое на ремонт мешалок, составляет 5 % от продолжительности цикла. [36]
 |
Нейтронный кон-центратомер серной кислоты. [37] |
Нейтронный метод определения концентрации особо чувствителен к колебаниям плотности кислоты и наличию примесей, поглощающих нейтроны. [38]
 |
Отношение коэффициентов р / А. Cg / p для серной и фосфорной кислот. [39] |
Нейтронный метод более значительно чувствителен к случайным колебаниям плотности кислоты, чем денсиметрический. [40]
Серная кислота непрерывно разбавляется водой; разбавление контролируется концентратомером по плотности кислоты. Затем через расходомер она поступает на смешение с апатитовым концентратом. [41]
При помощи термометра и, ареометра легко измерить температуру и плотность кислоты, а пользуясь результатами этих измерений и графиком, представленным на рис. 1 ( или таблицами, номограммой), установить концентрацию кислоты. [42]
Погрешность определения Ск складывается из погрешности определения Сн и колебаний плотности кислоты от изменения концентрации примесей, температуры и наличия взвесей и пузырьков газа. [43]
Погрешность определения концентрации кислоты зависит от погрешности нахождения С, колебания плотности кислоты, изменения состава и концентрации примесей, температуры кислоты, наличия пузырьков газа и механических частиц. Погрешность измерения нейтронного потока складывается из аппаратурной и статической погрешностей. [44]
Для растворов соляной кислоты установлена зависимость: если от числа, выражающего плотность кислоты, отнять единицу и полученную разность помножить на 200, то произведение с достаточной для практических целей точностью укажет на процентное содержание НС1 в данном растворе. [45]
Страницы: 1 2 3 4