Плотность - магний
Cтраница 1
 |
Диаграмма плавкости системы хлоридов калия, натрия, магния и кальция при постоянном содержании хлористого магния ( 10 %. [1] |
Плотность магния и карналлита находятся в пределах 1 6 - 1 7 г / см3, особенно они близки при температуре 700 С, наиболее удобной для электролиза. Аналогичная картина наблюдается и в тройных электролитах, содержащих MgCU, KC1 и NaCl. Это обстоятельство очень неблагоприятно для электролиза, так как образующиеся на катоде капли магния остаются в электролите, что создает условия обратного взаимодействия хлора с нагнием и, следовательно, приводит к бесполезным потерям электроэнергии. [2]
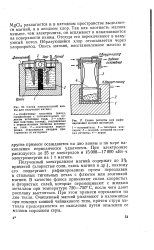 |
Схема электролизной ванны для получения магния.| Схема реторты для рафинирования магния возгонкой. [3] |
Так как плотность магния меньше, чем электролита, он всплывает и накапливается на поверхности ванны. Отсюда его перекачивают в вакуумный котел. Образующийся хлор отсасывается через хлоропровод. [4]
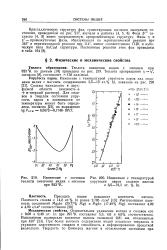 |
Изменение с составом [ IMAGE ] Изменение с температурой теплоты смешения индия с магнием упругости паров сплавов магния при 923 К. с 3 5 - 19 5 ат. % In. [5] |
Присадка индия повышает плотность магния. [6]
 |
Показатели работы магниевых электролизеров. [7] |
При недостаточной разности плотности магния и расплавленного электролита скорость вывода магния из зоны электролиза замедляется и могут возрасти его потери за счет реакции с хлором. Примеси, особенно сульфаты и влага, с которыми магний взаимодействует, способствуют его потерям. [8]
Плотность электролита поддерживают выше плотности магния 2, вследствие чего последний всплывает на поверхность, откуда периодически удаляется с помощью вакуумных ковшей и насосов. [9]
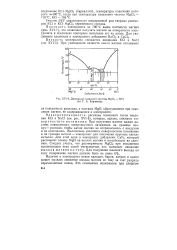 |
Диаграмма плавкости системы MgCl2 - КС1 ( по Г. А. Абрамову. [10] |
Плотность электролита до 700 С выше плотности магния ( рис. XVI-7), что позволяет получать магний на поверхности электролита и исключает повторное окисление его на аноде. [11]
Так как плотность расплавленного электролита больше, чем плотность магния при температуре электролиза, то выделяющийся на катоде жидкий магний, не растворяясь в электролите, в виде капель всплывает на его поверхность. На аноде выделяется газообразный хлор, который также поднимается и выбрасывается из электролита. Выделяющийся в анодной пространстве хлор отсасывают через трубы и используют, например, для хлорирования окиси магния или двуокиси титана. [12]
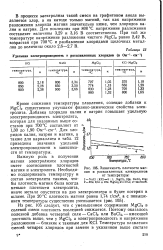 |
Зависимость плотности магния и расплавленных электролитов от температуры. [13] |
Важную роль в получении магния электролизом хлоридов имеет соотношение плотностей магния и электролита. [14]
Важную роль в получении магния электролизом хлоридов имеет соотношение плотностей магния и электролита. Необходимо поддерживать температуру и состав электролита такими, чтобы плотность магния была всегда меньше плотности электролита, иначе металл опустится на дно электролизера и будет потерян в шламе. [15]
Страницы: 1 2