Плотность - реакционная масса
Cтраница 2
Подобные процессы часто бимолекулярны, необратимы и, следовательно, кинетически протекают-по второму порядку. При проведении таких реакций в жидкой фазе плотность реакционной массы обычно не изменяется. [16]
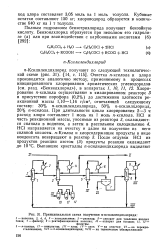 |
Принципиальная схема получения п-ксилилендихлорида. / - колонна. 2, 4, 6. 9 - холодильники. 3 - реактор. 5-аппарат для удаления кислых. [17] |
Очистка л-ксилола и хлора производится аналогично методу, применяемому в процессах инициированного хлорирования ароматических углеводородов ( см. разд. Хлорирование л-ксилола осуществляют в эмалированном реакторе 3 в присутствии порофора ( 0 2 %) до достижения плотности реакционной массы 1 10 - 1 16 г / см3, отвечающей следующему составу: 30 % л-ксилилендихлорида, 50 % л-ксилилхлорида, 20 % л-ксилола. При длительности цикла хлорирования 2 - 3 ч расход хлора составляет 1 моль на 1 моль л-ксилола. После отдувки НС1 из продуктов реакции азотом ( 5) продукты реакции охлаждают до 10 С. [18]
Это может быть оптическая плотность в видимой или УФ-областк спектра, давление насыщенного пара над реакционной массой, объем или плотность реакционной массы, диэлектрическая проницаемость, электропроводность, значение рН, объем поглощенного реакционной массой газа и др. При этом кинетические эксперименты удобнее проводить в такой области изменения концентраций реагента, где намеряемое физическое свойство линейно связано с концентрацией с реагента. Результатом кинетического эксперимента является в этих случаях зависимость какого-либо физического свойства реакционной массы от времени. При необходимости их легко пересчитать в зависимость концентрации от времени. Ниже приведено описание наиболее простых установок, используемых для измерения некоторых физических свойств реакционной массы в ходе реакции. [19]
Нейтрализация ведется следующим образом. К сульфомассе при перемешивании медленно приливают нагретый до 90 С 15 % раствор Сульфита натрия. После загрузки 80 - 85 % рассчитанного количества отбирают пробу для определения остаточной кислотности и плотности реакционной массы. [20]
Этот способ выражения очень удобен так как измерение объема пробы, зачастую отбираемой из нагретой смеси, не всегда возможно. Результаты расчета будут надежными при условии, что погрешности за счет удаления части реагентов из зоны реакции не больше ошибок анализа и что плотность реакционной массы в процессе превращения меняется незначительно. [21]
Наибольшее практическое значение имеет монохлорбензол. Однако подобрать такие условия, чтобы получать монохлорбензол без примеси полихлоридов, не удается. Поэтому процесс проводят в условиях, позволяющих получить возможно меньше полихлоридов. Конец реакции определяют по плотности реакционной массы. [22]
Условия перемешивания в реакторах для суспензионной полимеризации облегчаются из-за относительно невысокой вязкости реакционной массы, что снижает затраты энергии на перемешивание. Применение высокоинтенсивного перемешивания во время реакции нежелательно, так как это замедляет полимеризацию. Слишком медленное перемешивание приводит к чрезмерной агрегации полимера и к повышенной неоднородности его свойств. Так как плотность полимера несколько выше плотности реакционной массы, то при полимеризации стремятся избежать центрифугального эффекта и напрессовывания полимера на стенки реактора. [23]
В водяную баню с электрообогревом помещают круглодонную четырехгорлую колбу на 250 мл с барботером, мешалкой, термометром, обратным холодильником с газоотводной трубкой, соединенной с двумя последовательно присоединенными поглотительными склянками на 500 мл, заполненными водой ( 200 мл) и 20 % раствором NaOH. В колбу загружают 78 г безводного бензола и 1 г растертой в ступке в порошок чугунной стружки. При энергичном размешивании пропускают осушенный хлор ( см. синтез 2.6) со скоростью 150 - 200 мл / мин. Температура при этом повышается до 40 - 45 С. Плотность реакционной массы определяют, внося 1 - 2 капли в растворы HaSO4, ранее приготовленные. Если капля реакционной массы опускается на дно в первом растворе H2SO4 и плавает во втором, то хлорированная масса имеет нужную плотность и реакция считается законченной. Для удаления избытка СЬ и НС1 из реакционной колбы пропускают несколько минут аргон. Реакционную массу переносят в колбу Вюр-ца на 150 мл и при атмосферном давлении перегоняют, нагревая пламенем газовой горелки и собирая фракции, кипящие до 165 С, от 165 до 185 С и выше 185 С. Фракцию, кипящую в интервале 165 - 185 С, охлаждают в бане со смесью льда с поваренной солью, при этом 1 4-днхлорбензол выкристаллизовывается. [24]
По окончании загрузки происходит нейтрализация гидроокиси алюминия серной исло-той с образованием сульфата алюминия, при непрерывном пе-рем бшишиии реагирующей массы л аром или воздухом. Температура реагирующей массы поддерживается за счет теплоты, выделяемой при разбавлении серной иолоты водой и реакции нейтрализации в пределах 110 - i.40 C. Для этого по мере надобности в реактор подают воду. Для контроля процесса нейтрализации 2 - 3 раза берут пробу и определяют IB ней содержание свободной серной кислоты и окиси алюминия. По окончании реакции плотность реакционной массы доводят до 1 56 г / сии3 добавлением в реактор воды, подачу пара или воздуха прекращают и оставляют массу отстаиваться течение 20 - 25 мин. [25]
По окончаний загрузки происходит нейтрализация гидроокиси алюминия серной кислотой с образованием сульфата алюминия, при непрерывном пе-р вмешивании реагирующей массы л аром или воздухом. Температура реагирующей массы поддерживается за счет теплоты, выделяемой при разбавлении серной кислоты водой и реакции нейтрализации в пределах НО-il40 C. Для этого по мере надоб - fflocta в реактор подают воду. Для контроля процесса нейтрализации 2 - 3 раза берут пробу и определяют IB ей содержание свободной серной кислоты и окиси алюминия. По окончании реакции плотность реакционной массы доводят до 1 56 г / ом3 добавлением в реактор воды, подачу пара или воздуха прекращают и оставляют массу отстаиваться течение 20 - 25 мин. [26]
Для процессов жидкофазного окисления, имеющих целью получение гидроперекисей ( в частности, для получения гидроперекиси вгоуо-бутилбензола), Хчеяном предложен многоступенчатый реактор ( рис. III. Каждая ступень окисления составлена из трех вертикальных труб, сообщающихся между собой и образующих таким образом замкнутую циркуляционную систему. В две крайние трубы 2 подается через барботер воздух. Средняя труба является циркуляционной. Барботеры для распыления воздуха расположены ступенчато, с учетом изменения плотности реакционной массы по мере накопления в ней гидроперекиси. Такое расположение барботеров создает одинаковые гидростатические давления над уровнем ввода воздуха, а следовательно, и условия для равномерного распределения его по отдельным ступеням. [27]
В водяную баню с электрообогревом помещают круглодонную четырехгорлую колбу на 250 мл с барботером, мешалкой, термометром, обратным холодильником с газоотводной трубкой, соединенной с двумя последовательно присоединенными поглотительными склянками на 500 мл, заполненными водой ( 200 мл) и 20 % раствором NaOH. В колбу загружают 78 г безводного бензола и 1 г растертой в ступке в порошок чугунной стружки. При энергичном размешивании пропускают осушенный хлор ( см. синтез 2.6) со скоростью 150 - 200 мл / мин. Температура при этом повышается до 40 - 45 С. Через 2 ч хлорирования температуру реакционной массы повышают до. Плотность реакционной массы определяют, внося 1 - 2 капли в растворы H2SU4, ранее приготовленные. Если капля реакционной массы опускается на дно в первом растворе H2SO4 и плавает во втором, то хлорированная масса имеет нужную плотность и реакция считается законченной. Для удаления избытка С 2 и НС1 из реакционной колбы пропускают несколько минут аргон. Реакционную массу переносят в колбу Вюр-ца на 150 мл и при атмосферном давлении перегоняют, нагревая пламенем газовой горелки и собирая фракции, кипящие до 165 С, от 165 до 185 С и выше 185 С. Фракцию, кипящую в интервале 165 - 185 С, охлаждают в бане со смесью льда с поваренной солью, при этом 1 4-дихлорбензол выкристаллизовывается. [28]
Страницы: 1 2