Плотность - простое вещество
Cтраница 1
Плотность простых веществ повышается. [1]
Плотность простых веществ ряда кислород - теллур в твердом состоянии соответственно равна 1 4; 2 1; 4 8; 6 2, а температура плавления - 218 С; 119 С; 220 С; 450 С. Чем объясняется такая последовательность. Существует ли соответствие температур плавления с температурой кипения. [2]
Возрастание атомной массы в подгруппе приводит к увеличению плотности простых веществ, но вместе с тем к понижению точек плавления и кипения. Такое понижение вызвано уменьшением прочности химических связей между частицами соответствующих веществ. [3]
На рис. 125 - 127 показана зависимость от порядкового номера элементов плотности простых веществ в твердом состоянии, температуры их плавления и стандартной энтропии. [4]
 |
Плотность простых веществ.| Температура плавления простых веществ. [5] |
На рис. 144 - 146 показана зависимость от порядкового номера элементов плотности простых веществ в твердом состоянии, температуры их плавления и стандартной энтропии. [6]
На рис. 125 - 127 показана зависимость от порядкового номер а элементов плотности простых веществ в твердом состоянии, температуры их плавления и стандартной энтропии. [7]
АТОМНЫЙ ОБЪЕМ - объем 1 г-атома элемента; численно равен отношению атомной массы к плотности простого вещества в твердом состоянии. [8]
АТОМНЫЙ ОБЪЕМ - объем 1 грамм-атома элемента, равный частному от деления атомного веса на плотность простого вещества в твердом состоянии. Если элемент существует в нескольких аллотропич. [9]
Сказанное прежде всего относится к так называемым атомным объемам простых веществ, получаемым как частное от деления атомного веса на плотность соответствующего простого вещества. [10]
В свободном состоянии лантаноиды представляют собою типичные металлы, сходные с лантаном или с иттрием. В целом плотность простых веществ лантаноидов при переходе от Се к Lu на протяжении периода закономерно увеличивается ( от 6 7 до 9 85 г / см3) с увеличением массы атома. Это связано с тем, что атомы этих двух элементов имеют наполовину и полностью заселенные электронами 4 / - подоболочки, обладающие повышенной устойчивостью. Поэтому 4 / - электроны в образовании химической связи в простых веществах Ей и Yb почти не участвуют. Поэтому химическая связь обусловлена, в основном, только Gs-электронами и является менее прочной; атомы дальше располагаются друг от друга, а плотность простого вещества становится меньше. Оксиды лантаноидов нерастворимы в воде, но легко присоединяют воду с образованием гидроксидов. Последние лишь незначительно растворяются в воде и имеют основной характер. Соли лантаноидов по своей растворимости подобны соответствующим солям лантана или иттрия. [11]
Периодичность в изменении свойств элементов и их соединений позволяет вскрыть закономерности в проявлении элементом определенных не только химических, но и физических и механических свойств. Это объясняется плотной упаковкой атомов в металлических кристаллах, характеризующихся высокими значениями координационных чисел и большими массами самих атомов. При переходе к элементам концов периодов, к р-элементам, атомы которых склонны к объединению в молекулы, наблюдается понижение плотности простых веществ из-за более рыхлой структуры молекулярных кристаллов. [12]
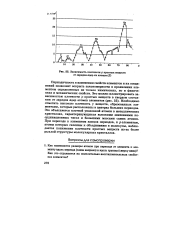 |
Зависимость плотности р простых веществ от зарядов ядер их атомов ( Z. [13] |
Периодичность в изменении свойств элементов и их соединений позволяет вскрыть закономерности в проявлении элементом определенных не только химических, но и физических и механических свойств. Необходимо отметить высокую плотность у веществ, образованных элементами, которые расположены в центрах больших периодов. Это объясняется плотной упаковкой атомов в металлических кристаллах, характеризующихся высокими значениями координационных чисел и большими массами самих атомов. При переходе к элементам концов периодов, к - элементам, атомы которых склонны к объединению в молекулы, наблюдается понижение плотности простых веществ из-за более рыхлой структуры молекулярных кристаллов. [14]
В свободном состоянии лантаноиды представляют собою типичные металлы, сходные с лантаном или с иттрием. В целом плотность простых веществ лантаноидов при переходе от Се к Lu на протяжении периода закономерно увеличивается ( от 6 7 до 9 85 г / см3) с увеличением массы атома. Это связано с тем, что атомы этих двух элементов имеют наполовину и полностью заселенные электронами 4 / - подоболочки, обладающие повышенной устойчивостью. Поэтому 4 / - электроны в образовании химической связи в простых веществах Ей и Yb почти не участвуют. Поэтому химическая связь обусловлена, в основном, только Gs-электронами и является менее прочной; атомы дальше располагаются друг от друга, а плотность простого вещества становится меньше. Оксиды лантаноидов нерастворимы в воде, но легко присоединяют воду с образованием гидроксидов. Последние лишь незначительно растворяются в воде и имеют основной характер. Соли лантаноидов по своей растворимости подобны соответствующим солям лантана или иттрия. [15]
Страницы: 1