Плотность - водород
Cтраница 1
Плотность водорода при нормальных условиях 0 0898 кг / м5, он самый легкий из всех известных газов и в 14 5 раз легче воздуха. [1]
Плотность водорода при тех же условиях примерно в 15 раз меньше, чем у азота. [2]
Определить плотность водорода, азота и кислорода на основании закона Авогадро при нормальных условиях. Найти плотность этих газов по водороду. [3]
Канниццаро плотность водорода принимает равной 2, отвергая как менее удобное приравнивание ее к 1 ( стр. [4]
Определить плотность водорода, азота и кислорода на основании закона Авогадро при нормальных условиях. Найти плотность этих газов по водороду. [5]
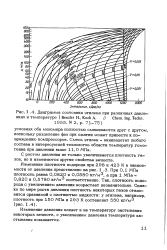 |
Диаграмма состояния этилена при различных давлениях и температуре ( Benzler H., Koch A. / / Chem. Ing. Techn. 1955. N 2, p. 71 - 75. [6] |
Изменение плотности водорода при 298 и 423 К в зависимости от давления представлено на рис. 1.3. При 0 1 МПа плотность равна 0 0820 и 0 0580 кг / м3, а при 1 МПа - 0 820 и 0 5780 кг / м0 соответственно. Так, плотность водорода с увеличением давления возрастает незначительно. [7]
Покончив с определением плотности водорода и кислорода, Рэлей занялся азотом. [8]
Плотность жидкого водорода значительно превышает плотность высококомпремирован-ного водорода ( при р 30 МПа р 0 0252 кг / л), что с точки зрения транспортных систем аккумулирования водорода представляет значительный интерес. Однако низкая температура, при которой возможно существование жидкого водорода, обусловливает жесткие требования к системам хранения по термо-статированию, технологии изготовления и применяемым материалам. [9]
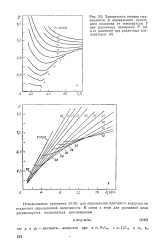 |
Зависимость степени сжимаемости б нормального газооб-ного водорода от температуры Т при различных давлениях Р ( а и от давления при различных температурах ( б. [10] |
Использование уравнения (3.19) для определения плотности водорода не исключает определенной погрешности. [11]
При температуре 7 - 10 К и плотности водорода 1 г / сма дейтерий все еще выгорает за время 10е лет. Поэтому в звездах выгорание дейтерия с превращением его в Не3 в огромной степени преобладает над образованием дейтерия. Таким образом, обычно считается, что D не может синтезироваться в заметных количествах ни в каких процессах в галактиках, а также в сверхмассивных объектах, если таковые имеются. Дейтерий может только разрушаться, как это имеет место, например, на Солнце. Поэтому считается, что весь D надо объяснять его синтезом в начале расширения горячей Вселенной. [12]
Однако помимо способности к сжижению, позволяющей увеличить плотность водорода в 836 раз, последний в отличие от метана может храниться в форме гидридов металлов. Цветные металлы, такие, как лантан или никелевые сплавы, могут селективно абсорбировать до 5 масс. % водорода при окружающей температуре и низких рабочих давлениях и высвобождать его при нагреве до определенного температурного уровня. [13]
Значительно снижается шум генерато-р а, так как плотность водорода невелика. [14]
Канниццаро предложил метод для вычисления молекулярной массы по удвоенной плотности водорода. Итальянский ученый, по-видимому, не знал, что за два года до этого, в 1856 г., Д. И. Менделеев вывел формулу M / D 2 для определения молекулярной массы Л / газообразных веществ по их плотности D и молекулярной массе воздуха независимо от знания химического состава вещества. [15]
Страницы: 1 2 3 4