Плотность - азот
Cтраница 1
Плотность азота рентгеновская при 50 К составляв. [1]
Найти плотность азота, если молекула за 1 с испытывает 2 05 108 с 1 столкновений при температуре 280 К. [2]
Значения плотности азота, брома, водорода, йода, кислорода, фосфора, фтора и хлора приведены для их естественного молекулярного состояния. [3]
Для определения плотности азота в среднем сечении регенератора применяют прямолинейный характер изменения температуры азота по длине регенератора. [4]
Разница в плотностях азота и кислорода настолько невелика, что для объяснения обсуждаемого феномена пришлось бы допустить фантастически большое содержание кислорода в очищенном азоте. [5]
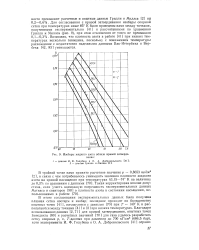 |
Изобары жидкого азота вблизи кривой затвердевания. [6] |
Возможно, что плотность азота в работе [41] при низких температурах несколько завышена, поскольку с понижением температуры расхождение с недостаточно надежными данными Ван-Иттербика и Вер-бека [42, 83] уменьшается. [7]
ГИ лученные значения плотности азота на кривой фазового равно весия приведены в интервале температур 120 - 126 16 К. [8]
Предварительные результаты экспериментального определения плотности азота приведены ниже в сопоставлении с данными таблиц [4], интерполированных к тем же значениям параметров. [9]
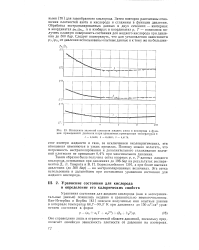 |
Отношение значений плотности жидких азота и кислорода в функции приведенного давления и при одинаковых приведенных температурах т. [10] |
Затем повторно рассчитаны отношения плотностей азота и кислорода и сглажены в функции давления. [11]
Я очень удивлен недавними результатами определения плотности азота и буду признателен, если кто-либо из читателей сможет указать причину. [12]
При 0 С и давлении 4 558 бар плотность азота равна 5 625 кг / мя. [13]
В 1893 г. было обращено внимание на несовпадение плотностей азота из воздуха и азота, получаемого при разложении азотистых соединений: литр азота из воздуха весил 1 257 г, а полученного химическим путем - 1 251 г. Произведенное для выяснения этого загадочного обстоятельства очень точное изучение состава воздуха показало, что после удаления всего кисло - рода и азота получается небольшой остаток газа ( около 1 %), который ни с чем химически не реагирует. Открытие нового газа, Названного аргоном ( по-гречески - недеятельный), представило, таким образом, торжество третьего десятичного знака. Так как молекула его одноатомна, атомный вес аргона равен молекулярному. [14]
В 1893 г. было обращено внимание на несовпадение плотностей азота из воздуха и азота, получаемого при разложении азотных соединений: литр азота из воздуха весил 1 257 г, а полученного химическим путем - 1 251 г. Произведенное для выяснения этого загадочного обстоятельства очень точное изучение состава воздуха показало, что после удаления всего кислорода и азота получался небольшой остаток ( около 1 %), который ни с чем химически не реагировал. Открытие нового элемента, названного аргоном ( по-гречески - недеятельный), представило, таким образом, торжество третьего десятичного знака. Так как молекула его одноатомна, атомный вес аргона равен молекулярному. [15]
Страницы: 1 2 3 4