Бромацетальдегид
Cтраница 1
Бромацетальдегид и глиоксаль реагируют с гетероциклами по атомам, участвующим в образовании водородных связей в двойной спирали ДНК. Модификации аденина и гуанинов свидетельствуют о нарушении двойной спирали и образовании однонитевых структур, в которых 11-аденин и 10 - и. [1]
В присутствии амида натрия 2-фенилпропионитрил алкили-руется диэтилацеталем бромацетальдегида. [2]
Исходные диацетали алкоксиацетальдегидов получаются из соответствующих диалкилацеталей бромацетальдегида, который, в свою очередь, получается бромированием паральдегида в спиртах. [3]
Бромирование паральдегида приводит к его трибромпроизводному, из которого бромацетальдегид получают путем перегонки в токе двуокиси углерода. [4]
Согласно методике Эрленмейера и сотрудников [2], 50 г деполимеризованного бромацетальдегида и 3 капли пиперидина добавляют к раствору 60 г тиобензамида в 180 мл абсолютного спирта. [5]
Головная фракция составляет 90 - 180 г и состоит главным образом из брома, бромацетальдегида и дибромацетальдегида. [6]
Необходимое для этого аминокарбонильное соединение-а-аминоацетальдегид-склонно давать различные побочные реакции, и по этой причине аминирование бромацетальдегида [27] и гидролиз амйноацеталя [8, 28] приводят лишь к очень низким выходам пиразина. [7]
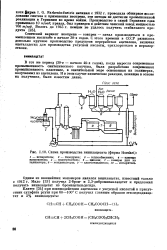 |
Схема производства винилацетата ( фирма Hoechst. [8] |
Одним из важнейших мономеров являлся винилацетат, известный только с 1912 г. Мило [33] получил 2-бром - и 2 3-дибромвинилацетат и предложил получать винилацетат из бромацетальдегида. [9]
Низшие алифатические альдегиды бурно реагируют с хлором и бромом; поэтому в реакциях галоидирования в качестве исходных веществ применяются их менее реакционноспособные полимеры. Так, для получения бромацетальдегида исходят из паральдегида. Хлорирование ацет-альдегида осуществляется лучше всего в присутствии сильной кислоты ( соляной, серной), полимеризующей сначала ацетальдегид в паральде-гид. [10]
Альдегидное строение продукта первого ряда превращений - хлормеркурацетальдегида было доказано весьма легко идущим восстановлением его при помощи изо-пропилата алюминия в соответствующий спирт п реакцией с трифенилхлорметаном, результатом которой был три-фенилметилацетальдегид. С бромом он почти количественно превращается в бромацетальдегид. [11]
На основании того, что конденсация тиосалициловой кислоты с бромацеталем совершенно не проходит в присутствии ацетата натрия, можно сделать заключение о малой подвижности атома галоида в бромацетале, для которого столь слабого конденсирующего средства, как ацетат натрия, оказывается недостаточно. Для проверки этого предположения была проведена конденсация тиосалициловой кислоты с бромацетальдегидом в присутствии ацетата натрия. [12]
Применив в качестве галогенокетона этиловый эфир бромпиро-виноградной кислоты, Борроус и Голланд синтезировали пирроколин-2 - кар-боновую кислоту ( LII, R - СО2Н) [77], которая при перегонке с окисью кальция была превращена в пирроколин. Повидимому, этот путь представляет лучший метод синтеза незамещенного пирроколина, так как реакция Чичибабина с бромацетальдегидом или его ацеталем не дает удовлетворительных результатов. [13]
После 5 мин кипячения на водяной бане реакционную массу выливают на лед, отделяют слой бромацеталя, из водного слоя последний извлекают эфиром. СОз - После отгонки эфира к этилового, спирта перегоняют диэтилацеталь бромацетальдегида на колонке в вакууме. [14]
К раствору 26 г диэтилового ацеталя хлормеркурацетальдегида в 50 мл сухого хлороформа при охлаждении и перемешивании прибавляют по каплям раствор 12 г брома в 30 мл хлороформа. Через несколько минут после прибавления брома ртутную соль отсасывают, осадок промывают хлороформом и от соединенных фильтратов отгоняют растворитель. При перегонке остатка получают 11 2 г ( 80 %) диэтилового ацеталя бромацетальдегида. [15]
Страницы: 1