Бромид - кальций
Cтраница 1
Бромид кальция СаВг2, СаВг2 - 6Н2О - белый порошок или извлекаемый из скважины рассол. Используют для приготовления солевых растворов повышенной плотности. [1]
Бромид кальция легко растворим в воде ( 595 г / 100 г Н20 при 0 С) и спирте. Кристаллизуется из воды в виде СаВг2 - 6Н20, плавящегося при 38 2 С. Известны также гидраты с 5; 4; 3; 2; 1 5 и 1 молекулами воды. Бромид кальция растворим в жидком аммиаке и этиловом спирте с образованием сольватов. [2]
Бромид кальция СаВг2 применяют как дегидратирующий агент, катализатор, активатор в ряде реакций, а также для получения тетрабромидов титана и циркония. Он находит применение и в медицине. [3]
Бромид кальция и бромид цинка редко применяют в лабораторной практике. [4]
Композиция бромид кальция - бромид цинка смешивается без ограничения с пресной водой и раствором бромида кальция. [5]
Растворы бромида кальция - бромида цинка представляют собой истинные растворы. Однако в связи с высокой концентрацией солей в растворе жидкости они не являются истинно ньютоновскими, а проявляют в некоторой степени дилатантные свойства ( рис. 20.6), т.е. с увеличением градиента скорости деформации вязкость в некоторой степени увеличивается, причем этот эффект наиболее заметен при невысоких температурах и в концентрированном растворе. При повышении температуры вязкость жидкостей падает, и эффект дилатантности уменьшается. То же происходит с разбавлением жидкости. [6]
Раствор бромида кальция в воде подвергается электролизу с платиновыми электродами. [7]
Взаимная пара бромид кальция - сульфат натрия по характе - 2Naci ру химического превращения относится к системам, практически односторонним. Поскольку-концентрации солей ( например, бромида кальция и сульфата кальция) различаются на 2 - 4 порядка, изображение такой системы взаимной пары очень затруднительно. Сложность пользования диаграммы возрастает вследствие необходимости вести с ее помощью технологические расчеты и изображать физико-химические превращения, происходящие в системе. Для таких случаев предложен метод изображения систем, состоящий в следующем. [8]
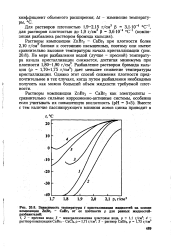 |
Зависимость температуры t кристаллизации жидкостей на основе композиции ZnBr2 - СаВг2 от ее плотности р для разных жидкостей-разбавителей. [9] |
Разбавление раствором бромида кальция ( р 1 70 - 5 - 1 75 г / см3) дает меньшее снижение температуры кристаллизации. Однако этот способ снижения плотности предпочтительнее в тех случаях, когда путем разбавления необходимо получить как можно больший объем жидкости требуемой плотности. [10]
Данные для бромида кальция. [11]
Обработка растворов бромида кальция плотностью до 1500 кг / м3 амилодекст-рином и крахмалом обеспечивает регулирование вязкости и фильтрационных свойств при температурах до 100 С. Свойства рассола плотностью до 1700 кг / м3 изменяются добавкой оксиэтилцеллюлозы. Этот реагент термостабилен до 150 С. Расход его значительно ниже, чем двух предыдущих. Фильтрационные свойства рассолов на основе бромида кальция хорошо регулируются комбинированным вводом оксиэтилцеллюлозы и карбонатов: мела, известняка, сидерита. [12]
В воде и спирте бромид кальция легко растворим. Эту соль применяют в фотографии и в медицине. [13]
При разложении 7 г бромида кальция СаВг2 получено 5 6 г брома. [14]
 |
Прибор для получения брома. [15] |
Страницы: 1 2 3 4