Расплавленный бромид
Cтраница 1
Расплавленные бромиды бериллия, бария, цинка, кадмия, ртути обмениваются с бромом быстро, а скорость обмена в комплексных бромидах типа KaHgBr4 ниже, значит, наличие брома во внутренней сфере комплекса затрудняет обмен с бромом. [1]
Расплавленный бромид иода как растворитель по свойствам очень похож на монохлорид иода, но стойкие кислоты в 1Вг пока не выделены. В бромиде иода это соединение ведет себя только как основание. [2]
Сначала расплавленный бромид этилпиридина, полученный смешением эквимолярных долей пиридина и этил-бромида в атмосфере азота, по каплям прибавляют к А1С1з в атмосфере азота или аргона. Полученное соединение растворяют в толуоле, вводят добавки и раствор перемешивают азотом или аргоном. Электролиз осуществляется с наложением переменного тока ( 400 пер / сек) на постоянный. Электролит перемешивают и непрерывно фильтруют воздушно-газовым насосом. [3]
В расплавленных бромидах и йодидах хлор при растворении вытесняет свободный галоген ( Вг2 или J2), который выступает в качестве непосредственного окислителя. [4]
В растворах расплавленного бромида ртути ( П) [160] многие реакции были исследованы кондуктометрически. Так, окись ртути ( П) можно легко протитровать перхлоратом ртути ( П) в расплавленном бромиде. [5]
Для этого каплю расплавленного бромида переносили при помощи тонкостенной стеклянной трубки на холодную пластинку из высокосиликатного стекла, которая моментально охлаждала гранулы и тем самым предупреждала возможность реагирования с кислородом атмосферы. [6]
Нами было измерено давление насыщенного пара над расплавленными бромидами иттрия и гольмия методом точки кипения [ ft ] в интервале температур Р20 - 1177 С. [7]
Бромиды электроположительных металлов, в том числе Т1, в расплавленном бромиде ртути ( П) ведут себя как типичные сольво-основания. [8]
В бромиде алюминия ( Ш) галогениды щелочных металлов обычно растворяются с образованием тетрабромоалюминатов; они также хорошо растворимы в расплавленном бромиде ртути ( П), из растворов которой могут быть выделены трибромоиеркураты. [9]
Бромид иода и бромид мышьяка ( Ш) как растворители очень похожи на монохлорид иода и хлорид мышьяка ( Ш) соответственно, но устойчивые кислоты из бромидных систем не были выделены. Расплавленный бромид ртути ( П) служит отличным растворителем для различных классов соединений. Бромиды щелочных металлов образуют сольватированные анионные частицы, которые, по-видимому, содержат ионы [ IBr2l -, [ AsBr4 ] - и [ HgBr3 ] - соответственно, а бромид фосфора ( У) в бромиде иода проявляет основные свойства и образует соединение PBr IBrj. Основные свойства в этих растворителях проявляет также пиридин. [10]
В растворах расплавленного бромида ртути ( П) [160] многие реакции были исследованы кондуктометрически. Так, окись ртути ( П) можно легко протитровать перхлоратом ртути ( П) в расплавленном бромиде. [11]
В связи с этим был разработан метод исследования химической сенсибилизации монокристаллов бромида серебра. Эти монокристаллы изготовлялись в виде тонких пластинок с плоскими, гладкими и параллельными поверхностями путем кристаллизации пленки расплавленного бромида серебра между двумя оптически отполированными пластинками из стекла пирекс. [12]
Радиусы анионов возрастают от F к J, и соответственно уменьшается сила взаимодействия ( стяжения) анионов расплавленной соли с катионами металлической фазы, способствующая ослаблению связи ионов металла с соседними и, следовательно, увеличению вероятности перехода их в расплавленную соль. Поэтому переход ионов металла в расплавленную соль с большей легкостью будет происходить в случае - расплавленных фторидов и хлоридов и с меньшей - в случае расплавленных бромидов и иодидов. В соответствии с этим электродные потенциалы металлов должны быть более отрицательны в расплавленных фторидах и хлоридах, чем в расплавленных бромидах и иодидах. Здесь, однако, как мы увидим ниже, имеются отклонения, обусловливаемые поляризацией ионов. [13]
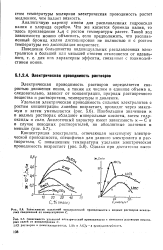
Что же касается бромида калия, то здесь произведение hur с ростом температуры растет. Такой ход зависимости можно объяснить, если предположить, что расплавленный бромид калия диссоциирован не полностью и с ростом температуры его диссоциация возрастает. [15]
Страницы: 1 2