Поведение - серебро
Cтраница 1
Поведение серебра в сорбционном процессе существенно отличается от поведения золота. При совместном присутствии в растворе золота и серебра сорбируется преимущественно золото. Поэтому проведение сорбции в режиме максимального насыщения смолы по золоту ведет к значительным потерям серебра. [1]
 |
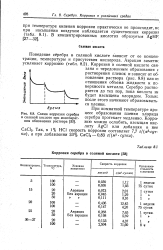
Зависимость поглощения разных элементов в пламени от расстояния до насадки на горелке. [2] |
Поведение серебра, которое не так легко окисляется, несколько иное - здесь наблюдается постоянное увеличение числа атомов, и абсорбционный сигнал больше, когда луч перемещается к периферии пламени. [3]
Поведение серебра в соляной кислоте зависит от ее концентрации, температуры и присутствия кислорода. Серебро растворяется до тех пор, пока кислота не l j будет насыщена хлоридом. [5]
Исследование поведения серебра и золота при электролитическом рафинировании меди с помощью радиоактивных изотопов этих металлов 78 показало, что серебро на 99 %, а золото на 100 % переходят в шлам, что последний, однако, катафорезом может быть перенесен на медный катод и тем легче, чем более вязок электролит, чем ближе расстояние между электродами и чем большую высоту имеют последние. Свинец и олово первично растворяются из медного анода и образуют сернокислые соли. [6]
 |
Теоретические области коррозии, невосприимчивости и пассивации серебра при 25 С. / - невосприимчивость. 2 - коррозия. 3 - пассивация. [7] |
Тремя основными факторами, определяющими поведение серебра в различных средах, являются высокая термодинамическая устойчивость этого металла, формирование на его поверхности пассивных защитных пленок и способность образовывать в растворах комплексные ионы. [8]
Из этих данных следует, что поведение золота в цианистых растворах отлично от поведения серебра и меди. [9]
Согласно Лалу и Тереку [185], поведение меди в нейтральных хлоридных растворах несколько отличается от поведения серебра. Как и в соляной кислоте [ НО, 111 ], в этом случае при низких плотностях тока медь растворяется благодаря относительной устойчивости растворимого хлоридного комплекса. Однако образование растворимых продуктов приводит в конце концов к осаждению ( при плотностях тока, превышающих 5 ма / см2) пленки полухлористой меди. [10]
Согласно Лалу и Тереку [185], поведение меди в нейтральных хлоридных растворах несколько отличается от поведения серебра. Как и в соляной кислоте [110, 111], в этом случае при низких плотностях тока медь растворяется благодаря относительной устойчивости растворимого хлоридного комплекса. Однако образование растворимых продуктов приводит в конце концов к осаждению ( при плотностях тока, превышающих 5 ма / см2) пленки полухлористой меди. [11]
В более поздних исследованиях по выяснению влияния аниона растворителя на свойства и устойчивость сереб-ра ( П) в кислых растворах [107] было обнаружено поразительное сходство в поведении серебра ( П) в средах хлорной, серной и фосфорной кислот. [12]
В серебре благоприятно сочетаются электрофизические, механические и другие свойства, что обеспечивает длительную надежную работу быстродействующих предохранителей при высокой плотности номинального тока и надежное отключение аварийного тока с требуемыми защитными характеристиками. Поведение серебра в различных средах характеризуется высокой термодинамической устойчивостью, формированием на его поверхности пассивных защитных пленок и способностью образовывать в растворах комплексные ионы. При температуре, меньшей точки плавления, серебро обладает значительной стойкостью к образованию оксида. В расплавленном серебре растворяется большое количество кислорода, которое при затвердевании выделяется из раствора в виде оксида серебра или рассеивается в металле в виде пузырьков. [13]
Страницы: 1