Поведение - вода
Cтраница 1
Поведение воды в системе углеводородов мало зависит от ее природы. Растворимость воды в углеводородах слабая и для расчета содержания паров воды в природном газе можно практически полагать, что она нулевая. [1]
Такое поведение воды в реакции с NH3 и HCN зависит от относительных величин сродства этих соединений к протону. Вещество, легко отдающее протон, называется сильной кислотой. Из двух веществ основанием будет то, которое активнее присоединяет к себе протон. По своей природе как вода, так и аммиак, могут играть роль основания. Однако из уравнения ( 2) видно, что при взаимодействии этих двух веществ основанием является аммиак, так как он активнее присоединяет к себе протон, образующийся при диссоциации воды. [2]
Такое поведение воды в реакции с NH3 и HCN зависит от относительных величин сродства этих соединений к протону. Вещество, легко отдающее протон, называется сильной кислотой. Из двух веществ основанием будет то, которое активнее присоединяет к себе протон. По своей природе как вода, так и аммиак, могут играть роль основания. Однако из уравнения ( б) видно, что при взаимодействии этих веществ основанием является аммиак, так как он активнее присоединяет к себе протон, образующийся при диссоциации воды. [3]
Для изучения поведения воды как вещества важно знать не только структуру ее молекулы, но и структуру молекулярных ассоциаций, связанных с высоким дипольным моментом каждой молекулы. Ориентируясь по отношению друг к другу противоположно заряженными полюсами и образуя при этом водородные связи, диполи воды способны обеспечивать ее структуру, отличающуюся высокой упорядоченностью молекул. Все эти особенности определяют уникальные свойства воды и особенности ее поведения как вещества. [4]
Тщательные исследования поведения воды показали, что хорошо известное понижение точки замерзания воды с увеличением давления наблюдается только в случае льда I до давления 2 2ПО am и температуры - 22 С. При более высоком давлении, чем указанное, температура плавления льда возрастает вместе с давлением. Бриджмен определил кривую плавления ( границу между твердым и жидким состояниями на диаграмме, где абсциссами служат давления, а ординатами-температуры) льда VI до давления, превышающего 20000 am, и температуры 76 - С. Температуры плавления льда III и VI возрастают вместе с давлением, подобно тому как при увеличении давления возрастают температуры плавления большинства материалов. Лед VI плавится при температуре 26 С под давлением 10 000 а. [5]
В детальном исследовании поведения воды на поверхности кремнезема, дегидратированного при 700 С, Клир и Цеттльмойер [23] показали, что молекула воды располагается на SiOH-rpyn - пах так, что ее атом кислорода направлен к группе ОН, по крайней мере на начальных стадиях адсорбции. Тогда водородносвя-занные кластеры, состоящие из молекул Н20, могут образовываться даже еще до того, как на всех SiOH-группах произошла адсорбция молекул Н20 и образовались поверхностные SisOH: ОН2 - группы. [6]
Наблюдения [106] за поведением воды и масла в стеклянном капилляре показывают, что при наличии на внутренней его поверхности хорошо смачивающей масляной пленки и при отсутствии перепада давления на концах капилляра распространяющееся на нее избыточное капиллярное давление вызывает отток масла из масляной пленки, уменьшая ее толщину. Наиболее заметное уменьшение тЪлщины пленки происходит вблизи мениска вследствие близости свободного объема и продолжается до тех пор, пока она не достигнет равновесного состояния. [7]
 |
Зависимость коэффициента вытеснения г трансформаторного масла из модели пласта водой от количества прокачанных поровых объемов воды. [8] |
Влияние электрического поля на поведение воды демонстрирует следующий опыт. При истечении из крана тонкой струйкой вода внизу дробится на капли. Рэлей показал, что это связано с тем, что возникающие при истечении возмущения распространяются вдоль струйки и усиливаются до тех пор, пока струйка не разрушается. При этом поверхностное натяжение заставляет жидкость собираться в капли. [9]
Изложенные закономерности подтверждаются энергетикой поведения воды на границе раздела фаз. Величина адсорбции С17 из водной среды равна 25 5 Дж / моль. При значениях PIPS 0 4 наблюдается образование моно -, а затем полимолекулярного слоя воды с ее дальнейшей конденсацией до P / PS 0 6, постепенно переходящей в состояние рыхлосвязанной ( обычной) воды. Это хорошо согласуется с данными по тепловым эффектам смачивания. Образованный вокруг частичек жесткоориентирован-ный слой ПАВ препятствует переходу воды в связанную. В глинистых капиллярах гидрофобный слой ПАВ способствует образованию менисков обратной кривизны, которые препятствуют перемещению капиллярной и гравитационной влаги; возникает противокапиллярное давление, уменьшающее передвижение рыхлосвязанной и фильтрацию свободной воды. [10]
Недавно сообщены первые результаты ЯМР-исследо-вания поведения воды в крахмале ( Lechert H. [11]
Пока имеется лишь качественная характеристика поведения пендулярной воды в пористых системах. Законы, регулирующие объем и поведение связанной воды в пластах, мало изучены, несмотря на то, что обычно весь коллектор содержит эту воду. Между тем тщательное исследование данного вопроса имеет огромное значение для подсчета запасов нефти, проектирования разработки месторождения и осуществления мероприятий по воздействию на пласт. [12]
Это утверждение основано на наблюдениях за поведением воды и масла в стеклянном капилляре. [13]
Как и во многих других отношениях, поведение воды представляет собой исключение. При низких температурах ее вязкость: повышением давления в отступление от общей нормы сперва падает и лишь в дальнейшем при более высоких давлениях и температурах начинает вновь возрастать. [14]
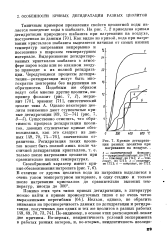 |
Кривые дегидратации разных цеолитов при нагревании на воздухе. [15] |
Страницы: 1 2 3 4